Tumori maligni dell’apparato muscoloscheletrico: concetti generali e classificativi
Reparto di Ortopedia e Traumatologia II, Università di Pisa
INTRODUZIONE
I tumori primitivi dell’apparato muscoloscheletrico sono estremamente rari rappresentando meno dell’1% della patologia oncologica. Interessano sia il genere maschile (1.3 casi/100000/anno) che quello femminile (1.1 caso/100000/anno). Pur nella loro rarità complessiva, essi presentano una notevole varietà di forme cliniche e istopatologiche, che interessano tutte le età (dalla prima infanzia all’età senile) anche se con incidenza diversa nei suoi vari istotipi.
In questo capitolo sulle generalità verranno presentati e illustrati i seguenti argomenti:
1. Recente (2020) Classificazione Istologica dei Tumori Maligni dell’osso secondo OMS.
2. Valutazione del grado istologico di malignità (Grading).
3. Valutazione dello stadio di estensione dei sarcomi (Staging):
a) modalità di crescita dei sarcomi;
b) classificazione AJC;
c) classificazione ENNEKING;
4. Valutazione Margini Chirurgici:
a) secondo AJC;
b) secondo Enneking;
c) secondo Kawaguchi.
5. Strategia chirurgica
6. Decalogo chirurgico
CLASSIFICAZIONE ISTOLOGICA DEI TUMORI MALIGNI DELL’OSSO SECONDO OMS (2020)
I tumori delle ossa e dei tessuti molli sono classificati secondo il tipo di tessuto predominante (pattern di differenziazione)3.
a. Tumori condrogenici
- Intermedio (localmente aggressivo)
- condromatosi, NAS;
- tumore cartilagineo atipico.
- Maligno
- condrosarcoma, grado 1,2,3;
- condrosarcoma dedifferenziato;
- condrosarcoma mesenchimale;
- condrosarcoma periostale;
- condrosarcoma a cellule chiare.
b. Tumori osteogenici
- Intermedio (localmente aggressivo)
- osteoblastoma, NAS.
- Maligno
- osteosarcoma centrale di basso grado;
- osteosarcoma, NAS;
- osteosarcoma convenzionale;
- osteosarcoma teleangectasico;
- osteosarcoma a piccole cellule;
- osteosarcoma parostale;
- osteosarcoma periostale;
- osteosarcoma superficiale di alto grado;
- osteosarcoma secondario.
c. Tumori fibrogenici
- Intermedio (localmente aggressivo)
- fibroma desmoplastico.
- Maligno
- fibrosarcoma, NAS.
d. Tumori vascolari
- Intermedio (localmente aggressivo)
- emangioma epitelioide.
- Maligno
- emangioendotelioma epitelioide, NAS;
e. Tumori osteoclastici ricchi di cellule giganti
- Intermedio (localmente aggressivo, raramente metastatizzante)
- tumore a cellule giganti dell’osso, NAS.
- Maligno
- tumore a cellule giganti dell’osso, maligno.
f. Tumori notocordali
- Maligno
- cordoma, NAS;
- cordoma condroide;
- cordoma scarsamente differenziato;
- cordoma dedifferenziato.
g. Altri tumori mesenchimali dell’osso
- Intermedio (localmente aggressivo)
- adamantinoma simile a displasia osteofibrosa;
- mesenchinoma.
- Maligno
- adamantinoma delle ossa lunghe;
- adamantinoma dedifferenziato;
- leiomiosarcoma;
- sarcoma pleomorfo, indifferenziato.
h. Neoplasie emopoietiche dell’osso
- plasmocitoma osseo;
- linfoma maligno, non-Hodgkin;
- malattia di Hodgkin, NAS;
- linfoma diffuso a grandi cellule B, NAS;
- linfoma follicolare, NAS;
- linfoma a cellule B della zona marginale, NAS;
- linfoma a cellule T, NAS;
- linfoma anaplastico a grandi cellule, NAS;
- linfoma maligno, linfoblastico, NAS;
- linfoma di Burkitt, NAS;
- istiocitosi a cellule di Langerhans, NAS;
- istiocitosi a cellule di Langerhans, disseminata;
- malattia di Erdheim-Chester;
- malattia di Rosai-Dorfmann.
i. Sarcoma indifferenziato a piccole cellule rotonde dell’osso e dei tessuti molli
- sarcoma di Ewing;
- sarcoma a cellule rotonde con fusioni EWSR1 non ETS9;
- sarcoma riarrangiato CIC;
- sarcoma con alterazioni genetiche BCOR
VALUTAZIONE DEL GRADO ISTOLOGICO DI MALIGNITÀ (GRADING)
La malignità cellulare viene valutata istologicamente mediante criteri generali (Anisocitosi e macrocitosi, Ipercellularità, Pleomorfismo cellulare) criteri citoplasmatici (iperbasofilia, vacuolizzazioni, secrezioni anomale, asincronia maturativa, cannibalismo) e criteri nucleari (anisocariosi e macrocariosi, aumento del rapporto nucleo: citoplasma(N:C), micronuclei, lobature nucleari – forme irregolari, multinucleazioni, aumento delle figure mitotiche, mitosi atipiche, pattern cromatinico immaturo, nuclear molding, anomalie dei nucleoli, nucleoli multipli)
Il grado istologico o grading, secondo la classificazione di Broder, rappresenta una misura del grado di aggressività o grado di differenziazione cellulare e quindi è strettamente legato alla prognosi. Questo parametro dunque descrive quanto il tumore si discosta istologicamente dal tessuto normale di partenza. Questo sistema di grading prevede 4 gradi possibili:
- GX Grado non determinato
- G1 Ben differenziato (basso grado): < 25% di cellule non differenziate;
- G2 Moderatamente differenziato (grado intermedio)< 50% di cellule non differenziate;
- G3 Scarsamente differenziato (alto grado) 50-75% di cellule non differenziate;
- G4 Indifferenziato Anaplastico. (alto grado): > 75% di cellule non differenziate.
Alcune classificazioni anziché 4 gradi di malignità, contemplano solo tre livelli :basso grado (grado 1 di Broder) intermedio (grado 2 di Broder)) alto grado (grado 3 e 4 di Broder). Altre (Henneking) prevedono solo due stadi: basso grado (grado 1e 2 di Broder) e alto grado (grado 3 e 4 di Broder)
VALUTAZIONE DELLO STADIO DI ESTENSIONE DEI SARCOMI (STAGING)
È evidente come un tumore con lo stesso aspetto istologico possa avere in pazienti diversi un diverso decorso clinico che va da una lesione indolente-statica ad un tumore aggressivo-maligno o addirittura metastatizzante.
Da qui la necessità di avere un sistema di stadiazione per:
- classificare i tumori in gruppi con comportamento e prognosi simili;
- produrre linee guida generali per il trattamento;
- avere un linguaggio comune per una valutazione più uniforme e confrontabile dei risultati oncologici.
Modalità di Crescita Tumorale
Crescita locale Si osservano due diverse modalità di crescita locale: “compressiva” o “infiltrativa”.
Il meccanismo compressivo è tipico dei tumori benigni, ma anche delle lesioni di grado molto basso. La compressione determina atrofia dei tessuti molli e dei muscoli circostanti e il riassorbimento dell’osso a causa dell’attivazione osteoclastica. Se il riassorbimento osseo così “indotto” avviene molto lentamente, si può osservare la contemporanea attivazione degli osteoblasti sul lato esterno della corticale riassorbita con nuova apposizione ossea. In questo caso l’osso può essere espanso ma conserva un guscio corticale periferico. Quindi un meccanismo di spinta può produrre una vera e propria “capsula” attorno al tumore dovuta a un sottile strato di normale tessuto fibroso o osseo maturo.
Il meccanismo infiltrativo è più frequente nei tumori maligni. Le cellule maligne possono svolgere un’azione sia diretta nella distruzione dell’osso circostante e dei tessuti molli sia indiretta mediante attivazione degli osteoclasti e crescere nell’area circostante formando digitazioni tumorali e satelliti. Questi focolai tumorali (satelliti) si propagano attraverso il reticolo venoso e possono indovarsi anche lontano dalla massa originaria (skip metastasi) senza una continuità diretta con il tumore, più spesso prossimalmente al tumore nello stesso compartimento o in un compartimento adiacente. A volte le skip metastasi possono essere trans articolari coinvolgendo l’osso adiacente. Le direzioni preferenziali e l’entità di crescita sono condizionate dalla aggressività cellulare della neoplasia (grading), dalla neoangiogenesi tumorale indotta, dalla reazione locale alla neoplasia, dalla presenza ed efficienza delle “barriere naturali” che si interpongono.
Reazione locale. Attorno ad un tumore si scatena una reazione locale molto simile alla fase infiammatoria del tessuto riparativo osservata nel processo di cicatrizzazione delle ferite o formazione dei calli. Nei tumori benigni e in alcuni maligni a bassissimo grado /border line la zona reattiva è costituita da a) edema, fibrina e infiltrazione di cellule infiammatorie; b) proliferazione delle cellule mesenchimali (istio-fibroblasti, osteoblasti) e dei vasi sanguigni; c) aree di tessuti preesistenti degenerati (muscolo, grasso) o riassorbiti (osso, cartilagine) d) aree cicatriziali. Peraltro nei tumori maligni in tale zona sono presenti anche nidi cellulari neoplastici, digitazioni tumorali e/o satelliti neoplastici. L’entità della reazione locale dell’ospite è correlata a diversi fattori: a) modalità e velocità di crescita del tumore (nella crescita permeativa di solito rapida si osserva una minore “reazione” da parte dell’ospite); b) entità di necrosi tumorale spontanea ed emorragia interna c) produzione di sostanze tumorali (fattori angiogenetici tumorali); d) risposta immunologica cellulare dell’ospite contro antigeni associati al tumore. Questa zona “reattiva” regredisce spontaneamente nella lesione benigna quando il tumore viene rimosso; mentre nelle lesioni maligne può diventare più spessa e matura quando il tumore viene devitalizzato da trattamenti preoperatori (chemio/radioterapia).
Incapsulamento. Il tumore d) può dunque essere incapsulato da: 1) un sottile strato di tessuto normale, causato dal meccanismo di crescita a spinta (capsula vera) e/o 2) una quantità variabile di tessuto reattivo. Poiché nei tumori maligni questo tessuto reattivo è riempito da digitazioni e satelliti tumorali, questo è considerato una pseudocapsula e rappresenta ovviamente un margine chirurgico non sicuro.
Risposta al trattamento neoadiuvante (chemio o radioterapico). Questa viene studiata dal confronto fra imaging iniziale (Rx. TC, RNM, Scintigrafia, PET) e imaging posttrattamento preoperatoria. Quando vi è buona risposta si assiste a:
- riduzione volumetrica del tumore (più evidente nello Ewing, meno nell’osteosarcoma);
- riduzione dell’edema peritumorale (RNM);
- aumento in spessore della pseudocapsula (TC, RNM);
- diminuzione della vascolarizzazione tumorale (scintigrafia trifasica, TC con mezzo di contrasto);
- aumento calcificazioni intra e peritumorali (Rx, TC);
- diminuzione dell’intensità di segnale in T2 (RNM)
- netto decremento della captazione alla PET (valore finale del SUV) e percentuale di decremento.
Barriere “anatomiche”. Kawaguchi (2004) ha classificato le strutture anatomiche che si oppongono alla crescita tumorale in:
barriere “forti”: rappresentate da:1) cartilagine articolare 2) fascia e setti fasciali 3) cartilagine di accrescimento 4) osso corticale 5) capsula articolare 6) strutture tendinee
barriere “relative”: rappresentate da :1) periostio 2) perinervio 3) avventizia vascolare 4) membrana sinoviale 5) guaine tendinee
barriere “deboli”: rappresentate da: 1) osso spongioso, 2) canale midollare, 3) la sottile corticale metafisaria (ove vi sono inserzioni capsulari e tendinee), 4) il grasso areolare presente nei piani fasciali e lungo i fasci neuro vascolari, 5) il muscolo, 6) lo spazio peridurale e 7) tutte le aree in genere in cui le barriere naturali sono perforate dai vasi nutritizi, la conoscenza di tali barriere naturali è fondamentale per la strategia chirurgica.
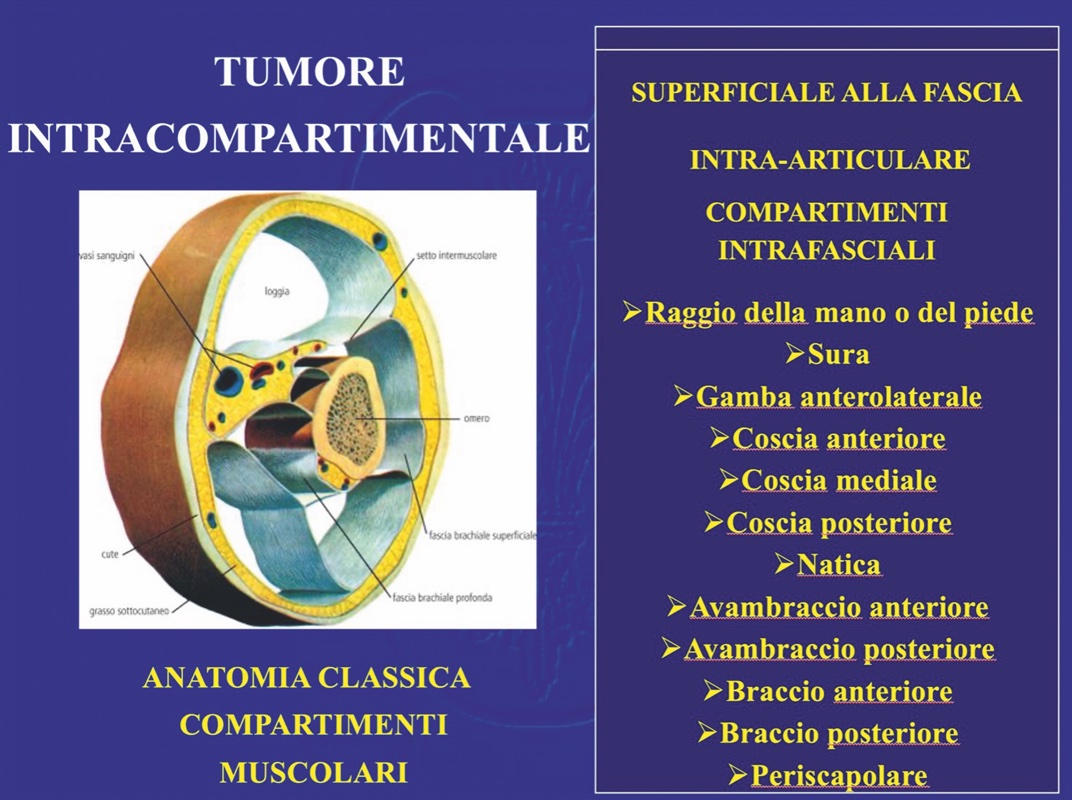
Compartimenti anatomici Enneking1,2 ha definito un compartimento come una struttura anatomica delimitata da barriere naturali (segmento osseo con il suo involucro periosteo, compartimenti muscolari delimitati da fasce e setti fasciali) che possono ostacolare la crescita tumorale e di tali strutture è stato fatto un elenco dettagliato Le neoplasie site in uno di tali compartimenti e incluse totalmente vengono definite a sede intracompartimentale. (Fig. 1).
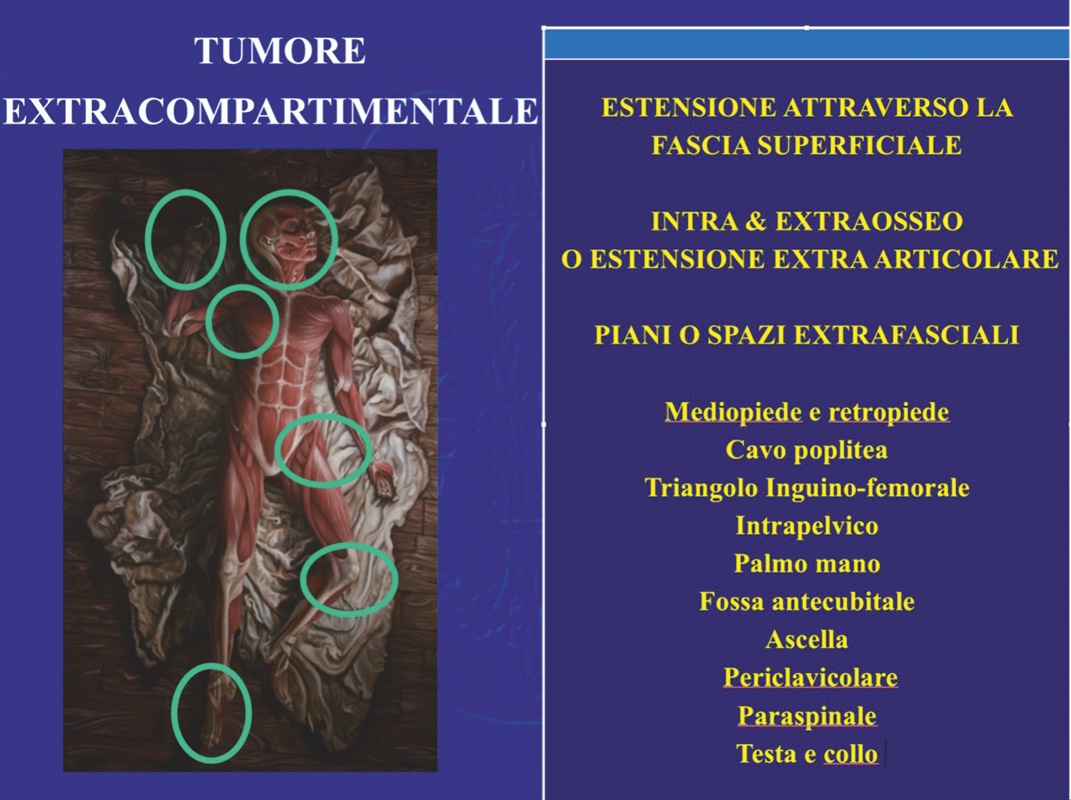
Tuttavia nel corpo umano esistono varie zone in cui questa separazione anatomica non esiste per cui si configura uno spazio in cui non vi sono barriere naturali all’espansione tumorale. Le neoplasie site in tali aree sono per definizione a sede extracompartimentale (Fig. 2)
Abbiamo visto peraltro che le barriere naturali possono essere suddivise in forti, relative (perché troppo sottili) e inefficaci (o a rischio). Se la barriera naturale è inefficace il tumore può perforarla e invadere il compartimento vicino o estendersi a una zona extracompartimentale : in tale caso il tumore da intracompartimentale diventa extracompartimentale. In realtà l’unica vera ed efficace barriera è la cartilagine articolare perché non presenta perforazioni vascolari e ha probabilmente una resistenza intrinseca al tumore. La neoplasia può tuttavia contaminare l’articolazione adiacente mediante diversi meccanismi:
- in seguito a una frattura patologica con coinvolgimento articolare;
- mediante infiltrazione dei legamenti (legamento rotondo -nell’anca o crociati nel ginocchio);
- estensione neoplastica attraverso le inserzioni epifisarie della capsula o della membrana sinoviale. (queste sono aree. a rischio perché in tali zone la corticale è molto sottile con multiple perforazioni vascolari per cui il tumore può facilmente estendersi dall’osso spongioso a tali strutture e viceversa;
- l’ulcerazione e il conseguente sanguinamento della membrana sinoviale possono produrre anche un emartro contenente cellule tumorali e conseguente contaminazione articolare.
Diverse forti barriere naturali come osso corticale, fascia e setti fasciali possono anche essere superate attraverso le loro perforazioni vascolari.
La cartilagine di accrescimento può fungere da barriera naturale all’invasione epifisaria e/o articolare tranne in caso di localizzazione intra articolare della stessa (come nell’anca) o nella prima infanzia o dopo l’età puberale, quando è perforata dai vasi. (comportamento analogo alla evoluzione in artrite settica di un focolaio osteomielitico metafisario).
Una biopsia malfatta (trasportando cellule tumorali da un compartimento all’altro, violando gli spazi extracompartimentali o articolari può trasformare un tumore intracompartimentale in uno extracompartimentale
Metastasi. Le metastasi si trovano solitamente nei polmoni perché i sarcomi ossei di solito metastatizzano attraverso il flusso sanguigno venoso. Inoltre l’interessamento dei linfonodi è raro perché l’osso è privo di vasi linfatici. Le metastasi linfonodali si osservano più spesso quando il tumore ha un’ampia componente di tessuto molle o coinvolge la cute (che al contrario è ricca di vasi linfatici). Questa occorrenza è però più comune nei sarcomi dei tessuti molli, in particolare nel sarcoma epitelioide, nel sarcoma sinoviale e rabdomiosarcoma.
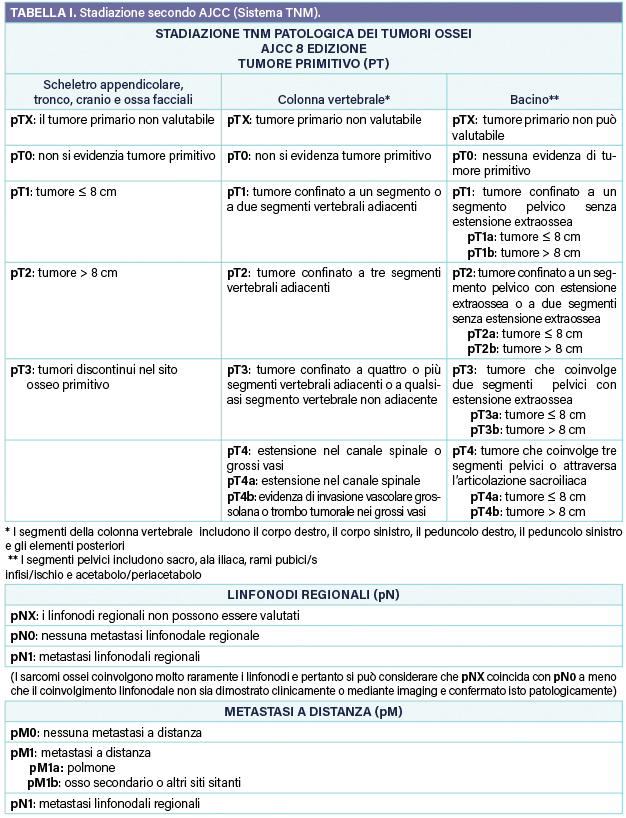
Stadiazione TNM dei Tumori Ossei. Classificazione AJCC (8°Edizione)
Questa classificazione a parte la constatazione o meno di metastasi linfonodali o a distanza per la valutazione dell’estensione locale tumorale prevede tre diverse situazioni (scheletro appendicolare, colonna vertebrale, pelvi). I criteri principali utilizzati sono stati: dimensioni e discontinuità tumorale (scheletro appendicolare); coinvolgimento progressivo dei vari segmenti vertebrali, estensione nel canale spinale, invasione vascolare / trombosi (colonna vertebrale) ; coinvolgimento progressivo dei vari segmenti pelvici, estensione extraossea, coinvolgimento articolare, dimensioni del tumore (bacino). Riguardo alle dimensioni del tumore il cut off è superiore o inferiore agli 8 cm (Tab. I)
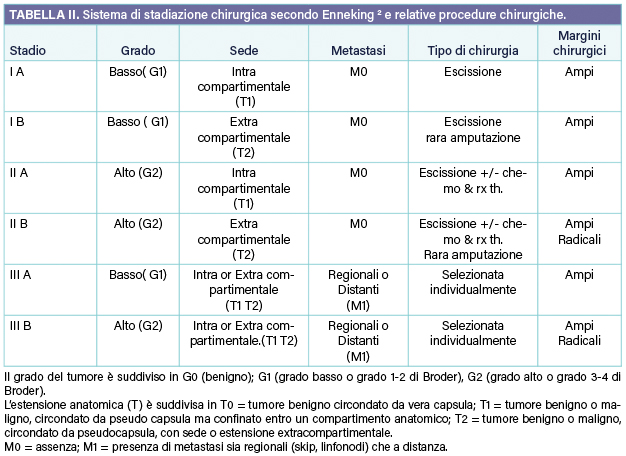
Sistema Di Stadiazione Chirurgica (Classificazione di Enneking)
I tumori sono stadiati classicamente in base al grado istologico (G), all’estensione anatomica (T) e alla presenza di metastasi regionali o a distanza (M). La stadiazione tiene conto anche di tutti i dati relativi agli studi clinici, di imaging e istologici.
I tumori benigni sono suddivisi in:
- Stadio 1 o lesione “latente”, “inattiva” che rimane statica o guarisce spontaneamente (come la maggior parte dei fibromi non ossificanti).
- Stadio 2 o lesione “attiva” che mostra una crescita progressiva ma limitata dalla barriera naturale (come la maggior parte dei tumori a cellule giganti).
- Stadio 3 o lesione “aggressiva” che presenta una crescita progressiva non limitata da barriere naturali (come alcuni tumori a cellule giganti pseudo maligni, cisti ossee aneurismatiche o osteoblastoma).
I tumori maligni si suddividono in:
Stadio I (basso grado), Stadio II (alto grado) o Stadio III (presenza di metastasi).
Inoltre, ogni stadio è suddiviso in A o B (a seconda dell’estensione intra o extracompartimentale del tumore).
A volte la stadiazione eseguita in fase preoperatoria (basata sulla biopsia) deve essere modificata dopo l’ampio studio dell’intero campione chirurgico (a causa della presenza di aree di dedifferenziazione o progressione di malignità).
MARGINI CHIRURGICI
I margini chirurgici dovrebbero essere valutati in sala operatoria sia dal chirurgo che dal patologo. Eventuali aree dubbie nel campo operatorio o nel campione resecato devono essere controllate mediante esame estemporaneo al congelatore. I margini ottenuti sono facilmente determinabili nel campione chirurgico se qualsiasi area sospetta è contrassegnata con inchiostro permanente. Diversi campioni per l’istologia vengono prelevati perpendicolarmente alla superficie marcata per valutare la quantità e la qualità dei tessuti che circondano il tumore.
Sistema R0, R1, R2 (AJC)
I margini vengono considerati liberi (R0) quando le cellule neoplastiche si trovano ad una distanza ≥ 2 mm dal margine nella sezione istologica, ma considerati esigui quando la neoplasia non infiltra il margine, ma si localizza in prossimità dello stesso, tra 1-2 mm dal margine della sezione istologica. Se il tumore si estende fino ai limiti della sezione istologica, la neoplasia viene definita infiltrante (margine “sporco”). L’infiltrazione del margine può essere ulteriormente classificata in infiltrazione focale R1 (con aggregati-propaggini di cellule neoplastiche ovvero residui microscopici di tumore) o come infiltrazione diffusa R2 (se vi sono residui macroscopici.
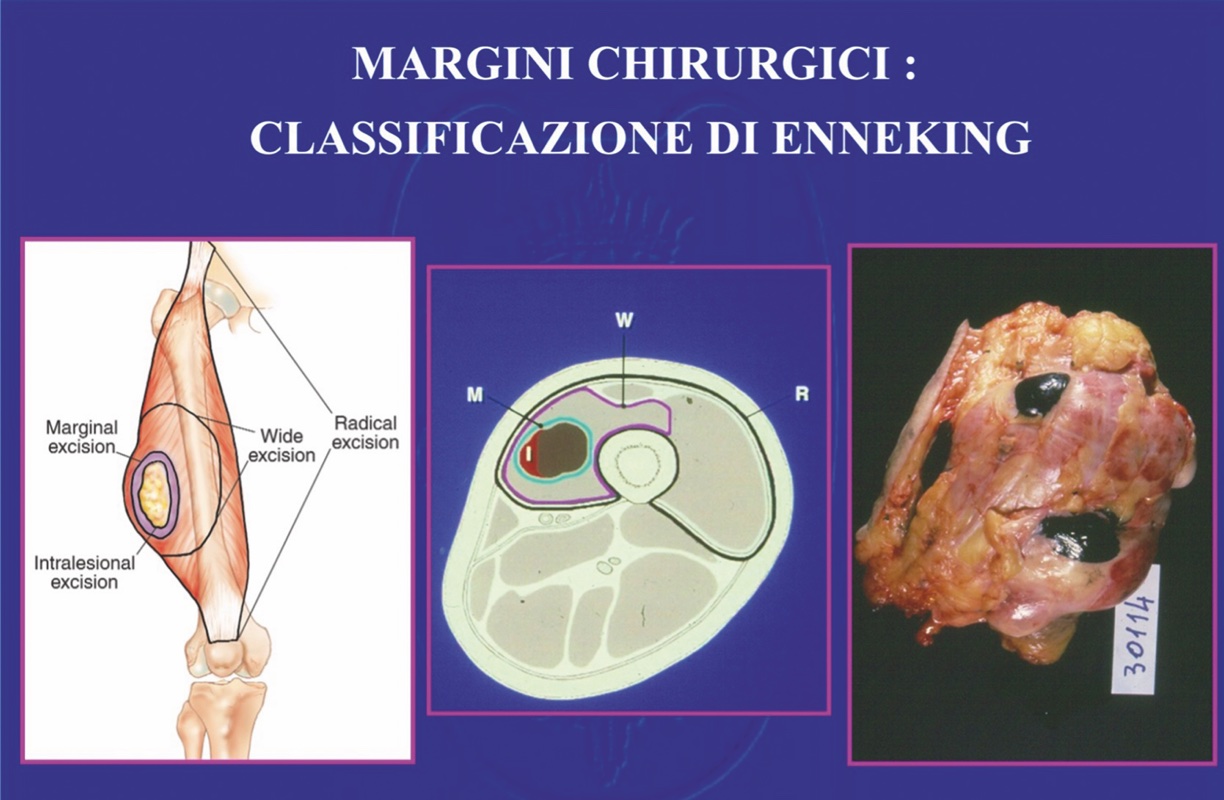
Classificazione secondo Enneking2
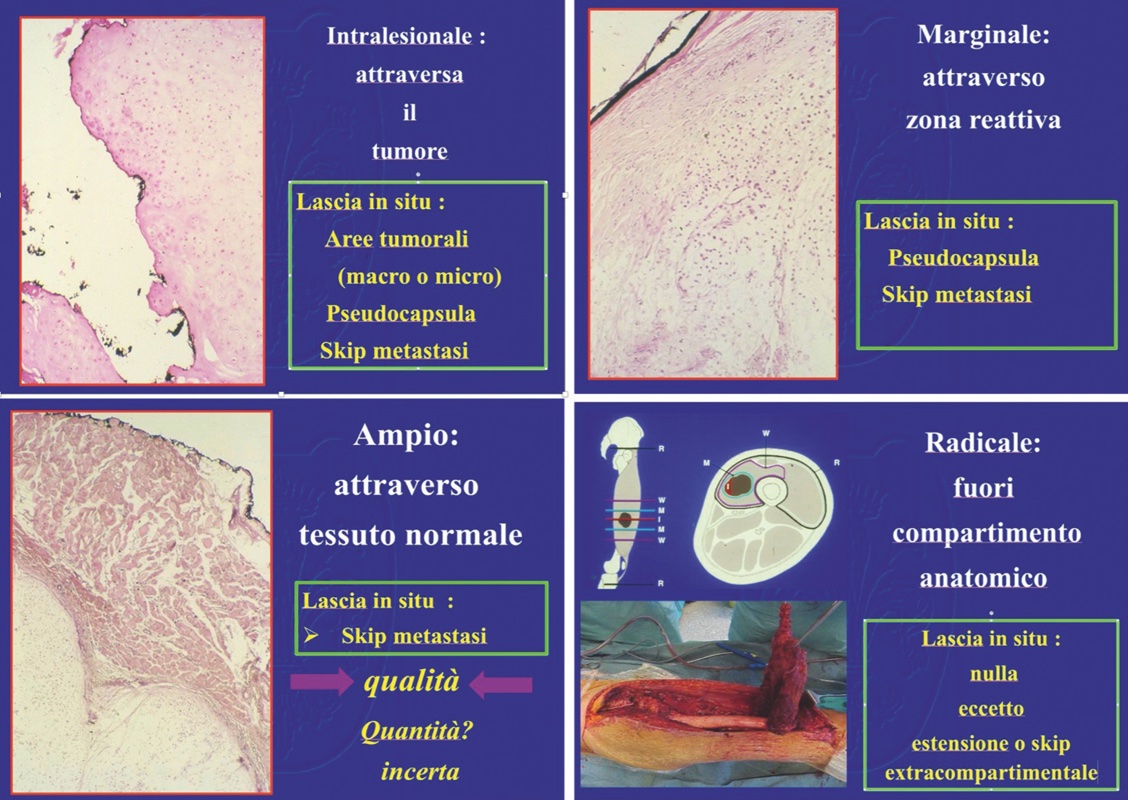
È più complessa ma anche più dettagliata. I margini vengono classificati in 4 categorie: 1) Intralesionale: quando si penetra nel tumore lasciando in situ macroscopiche aree residuali di malattia, la pseudocapsula ed eventuali skip lesioni 2) Marginale: quando il tumore viene rimosso in blocco ma seguendo un piano di dissezione che segue e sfrutta il piano di clivaggio della capsula o pseudocapsula tumorale (tecnica “shell out”). Tale procedura può essere adeguata nelle lesioni benigne ma, nei tumori maligni, lascia microscopiche aree residue di tumore nel campo operatorio. Queste sono rappresentate da cellule isolate o digitazioni neoplastiche presenti nello spessore della pseudocapsula, più possibili satelliti e skip lesioni locoregionali (spesso presenti nelle lesioni di alto grado); 3) Ampio: il tumore viene asportato in blocco tutto avvolto da una cuffia di tessuto normale. Questa procedura consente di rimuovere i satelliti attorno alla pseudocapsula ma può lasciare in situ skip lesioni locoregionali o trans articolari. Enneking non da un valore numerico allo spessore di tale cuffia di sicurezza, essendo per tale AA più legata alla tipologia del tessuto ricoprente che alla sua quantità o spessore: un piano fasciale di 1 mm sarebbe infatti una barriera più efficace di 2 cm di muscolo (concetto delle barriere anatomiche).Nei tumori ad alto grado (S.di Ewing, Osteosarcoma) il dominio su eventuali residui tumorali (skip lesion) non evidenziabili con le attuali tecniche di imaging in preoperatorio e lasciati in situ dall’intervento è affidato agli effetti delle chemio /radioterapie adjuvanti 4) Radicale: il tumore viene rimosso con l’intero compartimento (ad esempio una resezione totale del femore per un tumore intraosseo del femore distale; resezione totale del quadricipite per un sarcoma dei tessuti molli del vasto mediale; un’amputazione interscapolotoracica per un tumore del braccio eccetera.). Questa procedura è in grado di rimuovere anche skip lesioni, ad eccezione di quelle transarticolari. 5) Contaminato: una qualsiasi delle precedenti procedure deve anche essere chiamata “contaminata” se il chirurgo entra inavvertitamente nella lesione anche per una zona limitata e anche se successivamente riesce ad allargarne i margini nel tessuto normale.
Tale classificazione viene applicata sia per definire gli interventi conservativi (resezioni) sia quelli ablativi di amputazione. Per convenzione la procedura in toto è infine etichettata considerando solo il suo margine minore (ad esempio una resezione “ampia” che in un’area limitata mostra una pseudocapsula esposta sarà comunque definita “marginale”). Questo è un difetto della classificazione in quanto è intuitivo che il rischio di una recidiva locale è ben minore in una resezione ampia per il 90% e marginale nel restante 10% rispetto a una completamente marginale nel 100%. Per meglio definire i margini, essi dovrebbero essere analizzati non a random o solo su aree sospette ma su tutto il perimetro tumorale: attualmente questa indagine “perimetrale” viene raramente eseguita e non applicata di routine per lo sforzo organizzativo ed economico che essa richiederebbe. Un altro aspetto ancora insoluto è l’incidenza delle skip lesioni locali e dei satelliti nei vari tipi istologici e la determinazione della loro distanza media e di quella massima dal tumore: la conoscenza di tale dato potrebbe dare al chirurgo una indicazione quantitativa precisa (e non solo qualitativa) di quanto ampi (in cm) dovrebbero essere i margini ampi. Alternativa a ciò, il chirurgo dovrebbe poter contare in futuro su tecniche di imaging molto accurate che possano rilevare nidi anche microscopici di tumore, I margini attualmente suggeriti in relazione allo stadio del tumore sono riportati nelle tabelle III e IV secondo Simon4.
Classificazione secondo il metodo quantitativo di Kawaguchi5
Questa classificazione prevede margini intralesionali (curettage o debulking) e marginali (lungo la zona reattiva pericapsulare) del tutto sovrapponibili a quelli di Enneking. A differenza di Enneking, Kawaguchi prevede margini ampi suddivisi in ampi A (se vi è una cuffia di tessuto sano di 1cm -considerati peraltro inadeguati nelle forme ad alto grado) e in ampi B (se il tumore è circondato da una cuffia di tessuto sano tra 1 e 4 cm – considerati adeguati). Non esistono margini radicali (asportazione di tutto il compartimento anatomico) presenti nella classificazione di Enneking, ma vengono introdotti margini curativi (se il tumore è avvolto per oltre 5 cm di tessuto sano). Per il calcolo del “tessuto sano” circostante si avvale del concetto di equivalenza delle barriere naturali ovvero se circondato solo da una barriera debole (muscolo, grasso sottocutaneo, midollo osseo del canale midollare) in tali zone devono essere rispettate le distanze precedentemente date. Se peraltro si interpone una barriera intermedia (periostio, perinervio, avventizia vascolare, membrana sinoviale guaina tendinea) questa equivale a 2 cm di muscolo. Se si interpone una barriera forte (cartilagine articolare, cartilagine di accrescimento, capsula articolare, tendine, fascia o setti fasciali) queste strutture equivalgono allo spessore di 3 cm di muscolo. Questo approccio permette al chirurgo di eseguire uno studio preoperatorio basato sull’imaging delineando i piani di dissezione e determinando quali e quante strutture asportare per avere margini sicuri.
PIANIFICAZIONE CHIRURGICA
Nei tumori maligni l’obbiettivo del chirurgo è ottenere margini ampi (aree focali marginali sono accettabili solo nei tumori benigni o in quelli maligni con buona risposta al trattamento neoadiuvante e nell’intento di salvare importanti strutture funzionali). Eccezionalmente una resezione può ottenere margini radicali (scapulectomia, miectomia compartimentale, resezione ossea totale da articolazione ad articolazione).
Tratto bioptico e cicatrici precedenti
Vanno sempre rimosse, asportando un’ampia area ellittica di tessuti normali attorno ad esso. In caso di ampia rimozione cutanea per precedenti biopsie errate (incisioni multiple, parallele o trasversali) o nei tumori superficiali dei tessuti molli a volte si deve ricorrere a lembi peduncolati o liberi a scopo di copertura. Il sottocutaneo è diviso verso l’esterno in direzioni oblique e viene rimosso più ampiamente della pelle. La fascia sottostante viene ampiamente asportata e sfruttata come barriera anatomica.
Muscolo
Se il tumore è completamente intraosseo è sufficiente resecare l’osso in blocco con il suo periostio, sezionando a 0,5 cm di distanza dalle loro inserzioni tutti i setti, i tendini, i legamenti e coperto da un sottile strato di fibre muscolari inserzionali.
Al contrario il muscolo deve essere ampiamente resecato: a) su entrambi i lati del tragitto bioptico; b) a tutto spessore e su tutta l’estensione extraossea di un tumore osseo che ha le sue fibre inserzionali muscolari nella stessa area del tumore (es. il vasto intermedio o il vasto laterale per i tumori del femore distale); e tutt’intorno a un sarcoma dei tessuti molli. Questa cuffia di tessuto muscolare deve essere liberamente mobile, dall’aspetto normale e con uno spessore di almeno 2-3 cm. Una sezione tangenziale del muscolo (risparmiando la metà superficiale e lasciando a copertura solo la metà profonda) può essere eseguita solo da chirurgo esperto e in caso di buona risposta ai trattamenti preoperatori. Un atteggiamento più conservativo può essere utilizzato per quei muscoli che passano a ponte sull’area tumorale ma senza avere inserzioni dirette sull’osso interessato (es. il vasto mediale o il retto femorale per i tumori del femore distale).
Osso
L’estensione del tumore e la presenza di possibili skip nel canale midollare, nelle parti molli o transarticolari devono essere attentamente ricercate prima dell’intervento chirurgico mediante risonanza magnetica, scintigrafia ossea e P.E.T. Dovrebbe essere evidenziata anche la presenza di qualsiasi zona reattiva (e le sue variazioni prima e dopo i trattamenti preoperatori). La loro localizzazione va fatta prendendo misure da punti di riferimento facilmente riconoscibili anche intraoperatoriamente (apice gran trocantere, emirima articolare). Una biopsia supplementare può essere giustificata in aree di sospetta ma dubbia estensione tumorale. L’osteotomia deve essere eseguita in osso sano: ma la distanza ideale dall’apice del tumore (o zona edemato-reattiva, se presente) non è ancora ben definita Alcuni autori suggeriscono una zona di sicurezza di 7 cm. Personalmente utilizziamo 1 cm (nei benigni), 2 cm (nei bassi gradi) e 3 cm (negli alti gradi). Tuttavia, queste distanze di sicurezza possono essere aumentate (se non si prevedono effetti negativi sulla ricostruzione o sulla funzionalità) o diminuite per salvare importanti strutture anatomiche critiche (cartilagine di accrescimento o superficie articolare) o in presenza di una ottima risposta al trattamento preoperatorio. Il periostio viene esposto a livello dell’osteotomia programmata, marcato, tagliato e sollevato per un tratto limitato per poter passare due leve di protezione durante l’esecuzione dell’osteotomia con una sega oscillante. Dopo l’osteotomia il canale midollare deve essere immediatamente ispezionato per verificare la presenza di midollo osseo normale e un campione di questo deve essere prelevato ed inviato per esame estemporaneo. È fondamentale sezionare circonferenzialmente il periostio subito dopo l’osteotomia e prima di applicare qualsiasi trazione per evitare lo stripping accidentale dello stesso, con possibile violazione del tumore e contaminazione del campo chirurgico. Per analoghi motivi dopo l’osteotomia si applica una pinza ossea attorno al moncone del segmento da asportare bloccando il periostio sezionato sopra la corticale quindi lo spazio a livello dell’osteotomia viene aperto gradualmente al fine di sezionare i muscoli, i tendini e le inserzioni dei setti.
Un altro accorgimento può essere utilizzato nell’osteotomia iuxta-articolare transepifisaria. Diversi fili di Kirshner vengono inseriti parallelamente sotto guida radiografica per definire la linea dell’osteotomia. Questi fili fungono da guida potendo far scorrere su di essi un osteotomo o una sega oscillante: essi rappresentano dunque una barriera per prevenire una falsa direzione verso il tumore e minimizzare i rischi di una frattura accidentale della corticale posteriore che può estendersi verso il tumore o che può produrre uno sprone osseo danneggiando fascio vascolo-nervoso.
Articolazione
L’invasione articolare può essere sospettata in presenza di versamento, rigidità o dolore. La RNM è fondamentale nel valutare la crescita tumorale nelle inserzioni capsulari, nei legamenti e anche per dimostrare versamento o emartro. Una resezione intraarticolare è indicata se: 1) il bombé intrarticolare della lesione è minimo; 2) il tumore è ricoperto da un guscio osseo o almeno da una membrana sinoviale intatta; 3) capsula e legamenti sono solo parzialmente invasi;4) vi è minimo o assente versamento articolare. Solitamente la capsula e i legamenti devono essere sezionati nella loro parte intermedia per consentire la ricostruzione con un alloinnesto osteoarticolare, mentre possono essere asportati totalmente se si ricostruisce con una protesi vincolata. Una resezione extraarticolare è indicata se è presente: 1) contaminazione articolare secondaria a frattura patologica; 2) ulcerazione della membrana sinoviale con rigonfiamento macroscopico del tumore all’interno dell’articolazione o dei legamenti; 3) emartro massivo; 4) biopsia transarticolare; 5) origine intraarticolare del tumore (sarcoma sinoviale).
Fascio vascolare
Il rapporto tumore /vasi viene studiato mediante eco-doppler, C.T.con mezzo di contrasto o angio-M.R.I.; l’angiografia classica (più invasiva) è indicata quando, in caso di un by-pass già programmato, si richiedano informazioni sulla dimensione dei vasi e sulla sede dell’anastomosi.
I vasi compressi dal tumore vengono identificati a monte, preparati e retratti delicatamente con un vaseloop e quindi isolati in senso prossimo-distale. I vasi vengono salvati se è possibile una “dissezione smussa” usando un semplice tampone, retraendoli e legando solo i rami collaterali. Talora per allargare i margini chirurgici oltre all’areolare lasso può essere asportata l’avventizia che funge da discreta barriera. Se l’arteria non è coinvolta ma è difficoltoso dissociare la vena maggiore (o si osservano coaguli tumorali nei rami venosi collaterali) quest’ultima può essere sacrificata (senza ricostruzione) purché il circolo superficiale sia efficiente.
Se invece è richiesta una “dissezione strumentale” con forbici, i vasi devono essere resecati in blocco in quanto l’avventizia vascolare è diventata parte della pseudocapsula tumorale. Anche se alcuni Autori sono propensi a ricostruire la sola arteria (in quanto il by pass venoso tende a trombizzare nel tempo) in genere preferiamo ricostruire entrambe (arteria e vena) per i benefici effetti almeno nell’immediato e più critico periodo postoperatorio sulla circolazione sanguigna. Per evitare un by pass venoso profondo, occorre particolare cura nel preservare il circolo superficiale durante l’incisione cutanea e l’approccio al tumore. La ricostruzione biologica (autotrapianto di vena safena) è preferibile alle protesi artificiali tranne in caso di radioterapia postoperatoria. In passato il tasso di successo dei by-pass convenzionali sui vasi periferici distali al gomito o al ginocchio era limitato: l’introduzione di tecniche microchirurgiche avanzate ha permesso di superare tale limite.
Gli stessi criteri (dissezione “smussa” vs. “strumentale”) vengono utilizzati per decidere se rimuovere in blocco con il tumore dei visceri adiacenti e aderenti (ad esempio vescica o intestino nei tumori pelvici).
Trombi neoplastici nei rami venosi
È evento raro, osservato in tumori di grandi dimensioni con importante compressione del fascio vascolare principale. Purtroppo, tale evenienza è raramente rilevata preoperatoriamente anche utilizzando le più avanzate tecniche di imaging (T.A.C., R.M., angiografie), soprattutto se il fenomeno è limitato ai rami periferici senza coinvolgimento dei vasi maggiori. Il chirurgo può trovare rami venosi che provengono dall’area del tumore e confluiscono nei vasi maggiori ostruiti da trombi neoplastici: occasionalmente l’ostruzione può estendersi anche lontano all’interno della vena principale. Il riscontro di trombi neoplastici vasali, di consistenza dura, durante la legatura o il taglio dovrebbe allarmare il chirurgo e far richiedere una biopsia intraoperatoria estemporanea. Se i trombi neoplastici sono confermati, una dissezione più ampia (possibilmente con la rimozione dei vasi maggiori) o un’amputazione dovrebbe essere presa in considerazione.
Nervo
Raramente il nervo mostra forti aderenze con la pseudocapsula di un sarcoma. Paradossalmente questa eventualità si osserva più spesso nelle lesioni displastiche (fibromatosi, miosite ossificante). L’epinevrio, sebbene sottile, rappresenta una forte barriera anatomica all’infiltrazione tumorale. Per questo motivo il nervo viene isolato ed esposto dalla parte opposta alla lesione; l’epinevrio viene inciso longitudinalmente, e il nervo estratto dal suo involucro; l’epinevrio rimane così a copertura del tumore e viene rimosso in blocco con la lesione Questa tecnica è solitamente fattibile nei casi vergini ma difficilmente applicabile nei tumori recidivanti già sottoposti a precedente neurolisi o quando il nervo è incluso in tessuto cicatriziale e fibrosi. Quando il nervo è circondato dal tumore, va considerata una resezione segmentaria del nervo e ricostruzione mediante innesti nervosi, trapianto di unità motorie o trasferimenti di tendini. Se come metodo ricostruttivo si scelgono innesti nervosi, prima del taglio è utile mappare mediante stimolazione elettrica il nervo a livello della sezione prossimale e distale per riconoscere le fibre motorie e sensibili. Ciò aiuterà nella selezione delle priorità sull’innesto (spesso la disponibilità di innesti nervosi dopo un’ampia resezione dei nervi principali consente solo un ripristino anatomico parziale) e migliorerà notevolmente l’accuratezza e la qualità della ricostruzione. In caso di resezione nervosa maggiore (tronco sciatico, plesso brachiale, asportazioni multiple) vanno considerati i risultati funzionali attesi e confrontati con la funzione ottenibile con l’amputazione tenendo conto anche dell’adeguatezza oncologica della procedura chirurgica.
L’osso adiacente (sarcomi dei tessuti molli)
Se un tumore dei tessuti molli è in contiguità a un osso, per decidere se quest’ultimo va rimosso in blocco con la lesione vengono utilizzati i seguenti criteri:
- se il tumore è clinicamente mobile liberamente sul piano osseo e gli studi di imaging sono negativi, non è necessaria la rimozione dell’osso;
- se il tumore non è clinicamente mobile, la scintigrafia e gli studi di imaging sono negativi, si raccomanda la rimozione del tumore in blocco con il periostio adiacente;
- se si osserva una ipercaptazione scintigrafica dell’osso adiacente, senza segni di erosione ossea all’imaging è necessaria una parziale rimozione della corticale ossea, essendo il periostio coinvolto nella pseudocapsula tumorale;
- se la captazione della scintigrafia ossea è associata a reazione periostale o erosione corticale superficiale o edema all’interno del canale midollare è richiesta una completa rimozione in blocco dell’osso. La reazione periostale e l’erosione corticale sono meglio valutate dalla TAC., mentre l’edema midollare o le skip metastasi endomidollari vengono meglio rilevate mediante M.R.I;
- indipendentemente dall’imaging quando il tumore circonda completamente la diafisi si richiede l’asportazione in blocco dell’intero osso.
Se viene eseguita una rimozione estesa del periostio o una resezione ossea parziale, vi è un rischio maggiore di frattura patologica, in particolare se la radioterapia adiuvante è inclusa come parte del trattamento. In questo caso si dovrebbe prendere in considerazione un’osteosintesi profilattica di supporto e/o procedure di innesto osseo.
DECALOGO COMPORTAMENTALE DEL CHIRURGO
Usare l’imaging preoperatorio per pianificare mentalmente la configurazione tridimensionale del tumore e selezionando il piano di dissezione più appropriato.
Intraoperatoriamente, sentire i bordi del tumore con una palpazione delicata, senza esporre la pseudocapsula tumorale.
Modificare tempestivamente il piano di dissezione per aumentare i margini chirurgici se viene visualizzata l’area reattiva edematosa peritumorale.
Migliorare l’efficacia dei margini chirurgici includendo nel pezzo di resezione quante più barriere anatomiche intatte.
ln caso di barriere deboli e a rischio, cercare di massimizzare la quantità di tessuto sano rimosso attorno al tumore, compatibilmente alla procedura ricostruttiva selezionata e ai risultati funzionali desiderati.
Essere pronti a modificare o a passare intraoperatoriamente a metodiche ricostruttive diverse se l’adeguatezza dei margini chirurgici richiede una resezione più estesa di quella pianificata, con modifiche sulla fattibilità della ricostruzione.
Durante l’intervento eseguire un prelievo bioptico estemporaneo se si incontrano anomalie tissutali (edema, cicatrice, sospetti trombi).
Al termine dell’intervento controllare con campioni presi a random dal letto operatorio i margini chirurgici ottenuti e correggendoli immediatamente se non adeguati.
Scegliere una tecnica ricostruttiva anche ambiziosa ma non lasciare che quest’ultima condizioni l’appropriatezza oncologica della resezione.
Ricordarsi che questa patologia richiede un approccio multidisciplinare.
CAPITOLO 93Bibliografia.
- Enneking WF, Spanier SS, Goodman MA: A system for the surgical staging of muscoloskeletal sarcomas. Clin Orthop. 1980;153:106.
- Enneking WF. A system of staging muskuloskeletal neoplasms. Clin Orthop Relat Res. 1983;204:9-24.
- Capanna R. Le traitment des sarcomes des tissus mous. Cahiers d’enseignement de la SOFCOT 1998, pp. 175-189.
- Simon MA. Surgical Margins. In: Surgery for Bone and Soft Tissue Tumours. Ed. Simon Springfield, Lippincott-Raven 1998, pp.77-92.
- Kawaguchi N, Ahmed AR, Matsumoto S, et al. The concept of curative margin in surgery for bone and soft tissue sarcoma. Clin Orthop Relat Res. 2004 Feb;(419):165-72. doi: 10.1097/00003086-200402000-00027.