Protesi da grandi resezioni: tecnica chirurgica e complicanze
III Clinica Ortopedica a prevalente indirizzo Oncologico, Istituto Ortopedico Rizzoli, Bologna
Fino all’inizio degli anni ‘80, i sarcomi dell’osso venivano trattati nel 90% dei casi con tecnica demolitiva. Con il miglioramento delle tecniche diagnostiche e l’avvento della chemioterapia la chirurgia ricostruttiva con preservazione dell’arto è adesso possibile in 90%-95% dei pazienti con risultati in termini di sopravvivenza e di rischio di recidiva sovrapponibili all’amputazione1. L’aumento dei pazienti eleggibili per un intervento di salvataggio dell’arto e la maggior sopravvivenza dei pazienti stessi ha determinato crescenti esigenze ricostruttive, richiedendo soluzioni che permettano una buona mobilità, un buon risultato estetico e una lunga sopravvivenza dell’impianto.
PROTESI MODULARI DA RESEZIONE O MEGAPROTESI
Storia ed evoluzione delle megaprotesi
La ricostruzione con megaprotesi è stata per la prima volta descritta da Moore e Bohlman nel 1940, i quali hanno impiantato una protesi di femore prossimale su un paziente con un tumore a cellule giganti. Tuttavia, è solo intorno agli anni 70 che l’uso delle megaprotesi è comparso in letteratura e negli anni 90 diventarono sempre più popolari. Il principale vantaggio di una endoprotesi modulare è dato dal fatto che il chirurgo può concentrarsi sull’esecuzione della miglior resezione oncologica possibile sapendo che il cambiamento del piano operatorio può essere facilmente corretto selezionando le componenti che meglio si adattano al difetto scheletrico creato. Grazie alle componenti di prova modulari, il chirurgo può assemblare i segmenti in più varianti e testare la ricostruzione prima del montaggio della protesi definitiva.
Tecnica chirurgica
Tutte le protesi modulari sono costituite da questi tre elementi: gli steli, il corpo protesico con i vari estensori e la componente articolare (con le varie componenti in polietilene).
Il successo di un impianto protesico è dato da diversi fattori: il design della protesi, il tipo di articolazione ricostruita, la precisione della tecnica chirurgica e la modalità di fissazione dell’impianto. La fissazione dell’impianto avviene in due modi:
- Steli cementati: si utilizza in questo caso il cemento acrilico ed è ritenuta la più semplice ed economica tecnica di fissazione degli steli. Gli steli cementati sono soggetti, nel tempo, a maggiori complicanze di mobilizzazioni asettiche rispetto agli steli non cementati, a vantaggio però di un minor rischio di infezioni 2. In linea generale, in letteratura si raccomanda l’utilizzo di impianti cementati in pazienti con metastasi ossee, difetti osteolitici estesi dati ad esempio da lesioni linfoproliferative, pazienti con una prognosi scarsa e pazienti anziani osteoporotici che richiedono una mobilizzazione precoce.
- Steli non cementati: si basano sul fenomeno dell’osteointegrazione, un evento biologico che, grazie alle caratteristiche della superficie protesica, consente la formazione di un ampio contatto osso-protesi che determina la crescita di tessuto osseo che in questo modo stabilizza l’impianto. Si preferisce usare attualmente impianti non cementati soprattutto nei pazienti giovani 3.
Indipendentemente dalla sede del tumore, il tempo chirurgico prevede tre fasi:
- asportazione del tumore;
- ricostruzione del difetto con la protesi modulare;
- copertura della protesi con le parti molli.
L’asportazione del tumore può essere:
- intra-articolare: in questo caso viene effettuata una resezione attraverso l’articolazione, e questo è possibile nel caso in cui la neoplasia non abbia invaso la cavità articolare;
- oppure extra-articolare: in questo caso il tumore si è esteso anche all’interno dell’articolazione e per questo motivo l’intervento prevede la rimozione dell’intera articolazione.
In tutti i casi l’asportazione del tumore segue dei principi base che vano sempre rispettati: la cicatrice della biopsia va asportata insieme al tumore, la resezione va eseguita per via extraperiostea e nei casi in cui il tumore si estende fuori dall’osso bisogna asportalo senza esporre il tumore che deve rimanere avvolto da tessuto sano (asportazione con margini ampi).
Una volta completata l’asportazione del tumore il pezzo operatorio viene misurato per determinare le dimensioni del difetto che si è creato e per assemblare le componenti di prova che serviranno per fare le prove prima dell’impianto definitivo. Si procede quindi ad alesare il canale diafisario per l’impianto degli steli prescelti e si procede quindi a preparare l’articolazione adiacente per ricevere la protesi. Quindi la protesi di prova viene assemblata e impiantata. Il chirurgo valuta a questo punto, la lunghezza dell’impianto, la stabilita e l’articolarità. Eventuali dismetrie possono essere a questo punto corrette sostituendo le componenti con un segmento più lungo o più corto in base alla necessità. Una volta ottenute le dimensioni reali dell’impianto si procede ad assemblare la protesi definitiva che viene in seguito impiantata cementando o meno gli steli.
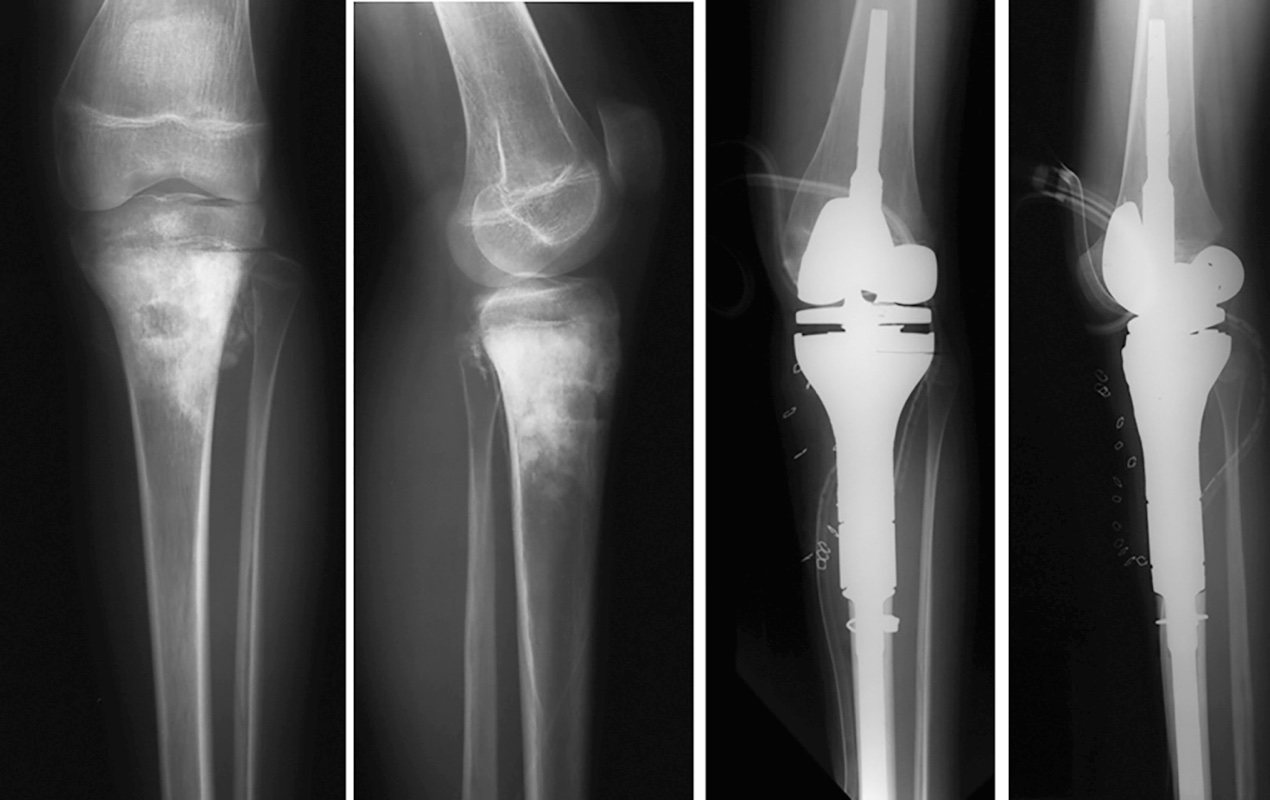
La terza fase prevede la copertura della protesi con i tessuti molli per consentire la necessaria stabilita e funzionalità della protesi. Una completa copertura della protesi e essenziale per minimizzare il rischio di deiscenza della ferita chirurgica e di sovra infezione. Per garantire un adeguata funzionalità della protesi i vari gruppi muscolari vano suturati direttamente alla protesi. Nel caso di protesi di femore prossimale è utile il mantenimento se possibile della capsula articolare. Se questo non è possibile, allora risulta fondamentale la reinserzione dei muscoli extra rotatori e dello psoas attorno alla testa femorale per creare una pseudocapsula e aumentare la stabilità dell’impianto. Inoltre, gli abduttori vano reinseriti a livello della parte trocanterica della protesi per migliorare la deambulazione e ridurre il trendelenburg. A livello del ginocchio e soprattutto nelle ricostruzioni di tibia prossimale risulta fondamentale la rotazione del muscolo gemello mediale a copertura della protesi, consentendo anche la sutura diretta del tendine rotuleo su questo muscolo, che risulta fondamentale per mantenere la funzionalità estensoria del ginocchio (Fig. 1).
Complicanze delle protesi modulari
In ambito oncologico l’incidenza di complicanze e fallimento delle protesi risulta maggiore rispetto alle protesi convenzionali, in relazione alle peggiori condizioni del paziente (immunosoppressione dovuta alla chemioterapia) e alla necessità di dover resecare una maggior quantità di tessuto osseo e parti molli per asportare il tumore con margini chirurgici adeguati.
Una prima distinzione va fatta tra complicanze meccaniche e non meccaniche.
Le complicanze meccaniche comprendono cause che vedono compromessa l’integrità della protesi stessa, dell’osso e dei tessuti molli peri-protesici: appartengono a questo gruppo il fallimento strutturale, la mobilizzazione asettica, le problematiche dei tessuti molli peri-protesici e la lussazione.
Le cause non meccaniche comprendono l’infezione e la progressione tumorale.
Queste complicanze sono state raggruppate in diverse classi grazie alla classificazione elaborata nel 2011 da Henderson 4.
Tipo 1: “soft tissue failure”
I fallimenti funzionali sono quelli che determinano disfunzioni dovute a instabilità dell’impianto che portano alla sublussazione e lussazione dell’impianto. La lussazione dell’impianto rappresenta una complicanza frequente nel caso di protesi dell’omero prossimale con incidenza variabile in letteratura tra il 1%-20% mentre a livello del femore prossimale la lussazione ha un incidenza variabile tra il 2 al 30%.
Tipo 2: “mobilizzazione asettica”
L’allentamento asettico convenzionale si manifesta come riassorbimento osseo peri-protesico mediato da osteoclasti, solitamente dovuto a detriti microscopici di polietilene, che tipicamente si presenta diversi anni dopo l’intervento. Anche una scarsa tecnica chirurgica può favorire la mobilizzazione dell’impianto, ad esempio, un sottodimensionamento degli impianti non cementati o scarsa tecnica di cementazione per impianti cementati. I pazienti sottoposti a trattamenti adiuvanti per malattia oncologica possono presentare una forma precoce di mobilizzazione asettica risultante da una scarsa crescita ossea e dalla formazione di una giunzione fibrosa nell’interfaccia osso-impianto. I dati in letteratura mostrano un’incidenza di tale complicanza variabile tra il 4.9%-9.6% 5.
Tipo 3: “cedimenti strutturali dell’impianto”
Fanno parte di questo gruppo l’usura o le rotture dell’impianto che richiedono una revisione e le fratture peri-protesiche.
Le fratture peri-protesiche si verificano più comunemente nei pazienti con osteoporosi o di età più avanzata, ma possono essere anche di natura traumatica. In base alla natura, della sede , o dell’impianto coinvolto può essere necessario un nuovo intervento di sintesi della frattura oppure nei casi più complicati anche di sostituzione di una componente dell’impianto o di tutto l’impianto. In una metanalisi pubblicata di recente in letteratura il tasso di complicanze di tipo 3 è stato di 6.35% per il femore distale mentre nella tibia prossimale variava da 2% a 12% 6.
Tipo 4: “infezioni”
La complicanza settica rappresenta una delle principali cause di fallimento per le protesi.
I principali fattori di rischio per infezioni peri-protesiche sono legati: alla complessità della resezione stessa con asportazione massiva di osso e tessuti molli, lunghi tempi operatori e condizioni debilitate e immunodepressione del paziente derivata dalla chemioterapia.
Mentre la manifestazione clinica di una infezione non differisce da quelle si evidenziano nelle protesi standard, il trattamento in questi casi e più complicato 7. L’esame più accurato per la diagnosi è l’esame chimico-fisico del liquido articolare associato ai valori di PCR sierici. La presenza di una fistola è segno certo di infezione peri-protesica e non richiede altri accertamenti radiologici di secondo livello. Mentre la scintigrafia ossea con leucociti marcati, per aiutare nella diagnosi differenziale tra mobilizzazioni asettiche e settiche 8.
Le misure terapeutiche a disposizione in caso di accertata infezione peri-protesica sono: la pulizia chirurgica “one stage” o la pulizia chirurgica “two-stages” con espianto completo della protesi e confezionamento di spaziatore in cemento antibiotato.
La prima è indicata nei casi di infezione “precoce” ossia entro i 30-40 giorni dall’intervento chirurgico o dall’inizio dei sintomi in caso di infezione da disseminazione ematogena. Essa consiste in un’apertura completa della cicatrice chirurgica con accurata pulizia chirurgica dell’impianto protesico e dei tessuti peri-protesici, svuotamento di eventuali ematomi, eventuale sostituzione delle componenti in polietilene con l’esecuzione di diversi prelievi per esame istologico e colturale. Dopo tale intervento chirurgico il paziente eseguirà una terapia antibiotica inizialmente ad ampio spettro (se il patogeno non era stato precedentemente isolato) e poi mirata sulla base dei riscontri dell’esame colturale intraoperatorio
Nelle forme croniche invece l’espianto completo della protesi con posizionamento di spaziatore in cemento antibiotato e successiva riprotesizzazione (tecnica “two-stages”) risulta più efficace. L’espianto della protesi è la premessa alla guarigione in tutte le infezioni croniche; resta inoltre il trattamento da perseguire negli insuccessi del trattamento di pulizia chirurgica “one stage”. Lo spaziatore ha la funzione di impedire l’adesione dei capi articolari, mantenere la lunghezza dei muscoli e ridurre il rischio di raccolta ematica articolare post-operatoria, rilasciando contemporaneamente antibiotico nel focus infiammatorio. L’impianto di una nuova protesi è possibile con la normalizzazione degli indici di flogosi (VES, PCR), la negativizzazione degli esami colturali e della conta leucocitaria almeno a 2 settimane dalla sospensione dell’antibiotico.
Tipo 5 “Recidiva del tumore”
La recidiva del tumore rappresenta la complicanza più temibile in caso di sarcomi dell’osso in quanto influisce negativamente sulla prognosi del paziente. Per liberare il paziente dalla malattia, molto spesso e necessario un intervento di amputazione.
CAPITOLO 95Bibliografia.
- Campanacci M. Bone and Soft Tissue Tumors. Springer; 2013.
- Coathup MJ, Sanghrajka A, Aston WJ, et al. Hydroxyapatite-coated collars reduce radiolucent line progression in cemented distal femoral bone tumor implants. Clin Orthop Relat Res. 2015 Apr;473(4):1505-14. doi: 10.1007/s11999-014-4116-6.
- Batta V, Coathup MJ, Parratt MT, et al. Uncemented, custom-made, hydroxyapatite-coated collared distal femoral endoprostheses: up to 18 years’ follow-up. Bone Joint J. 2014 Feb;96-B(2):263-9. doi: 10.1302/0301-620X.96B2.32091.
- Henderson ER, Groundland JS, Pala E, , et al. Failure mode classification for tumor endoprostheses: retrospective review of five institutions and a literature review. J Bone Joint Surg Am. 2011 Mar 2;93(5):418-29. doi: 10.2106/JBJS.J.00834.
- Brown IW, Ring PA. Osteolytic changes in the upper femoral shaft following porous-coated hip replacement. J Bone Joint Surg Br. 1985 Mar 1;67-B(2):218-21. doi: 10.1302/0301-620X.67B2.3980529.
- Pala E, Trovarelli G, Calabrò T et al. Survival of modern knee tumor megaprostheses: failures, functional results, and a comparative statistical analysis. Clin Orthop Relat Res. 2015 Mar;473(3):891-9. doi: 10.1007/s11999-014-3699-2.
- Lewis SS, Dicks KV, Chen LF, et al. Delay in diagnosis of invasive surgical site infections following knee arthroplasty versus hip arthroplasty. Clin Infect Dis Off Publ Infect Dis Soc Am. 2015;60(7):990-6. doi: 10.1093/cid/ciu975.
- Lee YS, Koo K-H, Kim HJ, et al. Synovial Fluid Biomarkers for the Diagnosis of Periprosthetic Joint Infection: A Systematic Review and Meta-Analysis. J Bone Joint Surg Am. 20 dicembre 2017;99(24):2077-84. doi: 10.2106/JBJS.17.00123.