Revisione di protesi di spalla
Università degli Studi di Pavia; Fondazione I.R.C.C.S. Policlinico San Matteo – Pavia
INTRODUZIONE
L’incidenza di revisioni di protesi di spalla è aumentata in modo rilevante negli ultimi anni non solo per il corrispettivo aumento di impianti primari, ma anche per il netto miglioramento della prognosi funzionale dei reimpianti rispetto a pochi decenni fa. Questo dato è correlato all’introduzione e alla diffusione della protesi inversa nella pratica clinica, un evento che ha parzialmente sovvertito il concetto di “chirurgia dei tessuti molli”, che era ed è ancora uno dei principi guida della protesizzazione anatomica.
Fino al nuovo millennio il risultato funzionale di una protesi di spalla (anatomica) era fortemente influenzato dal quadro anatomo-patologico di partenza. Un grave sovvertimento anatomico dei capi articolari (ad es. nelle viziose consolidazioni delle fratture dell’omero prossimale) o una compromissione strutturale o funzionale della cuffia (ad es. nelle rotture massive con coinvolgimento del tendine sottoscapolare) erano quasi inevitabilmente destinate a esitare in uno scarso recupero dell’articolarità attiva della spalla.
La “rivoluzione” biomeccanica introdotta dalla protesi inversa ha modificato in modo radicale questo scenario, rendendo possibile, per lo meno in termini di recupero dell’elevazione attiva, risultati dapprima inimmaginabili. Questo ha naturalmente avuto una ripercussione sugli interventi di revisione protesica, molto spesso caratterizzati da compromissioni anatomo-funzionali dell’articolazione scapolo-omerale che non potevano essere affrontati in modo efficace con i tradizionali impianti anatomici1. Va tuttavia sottolineato che questi ultimi hanno ancora un ruolo nelle procedure di revisione, qualora le perdite di bone stock siano contenute e l’integrità della cuffia sia ancora conservata nei suoi elementi essenziali.
Per comodità di trattazione il capitolo è stato suddiviso in tre sezioni. La prima è dedicata a una breve analisi delle cause di fallimento delle protesi di spalla, mentre le ultime due descrivono le problematiche specifiche della revisione della componente omerale e di quella glenoidea (sotto l’aspetto prettamente chirurgico, senza trattare le implicazioni infettivologiche proprie delle protesi settiche). Questa suddivisione non vuole esprimere una disgiunzione tra questi argomenti, poiché tutti devono essere presi in considerazione contemporaneamente nella pianificazione e realizzazione dell’intervento di revisione.
EZIOLOGIA
I fallimenti delle protesi di spalla traggono origine da svariate cause, le cui rispettive incidenze tendono a essere dissimili in relazione al tipo di impianto primario. I dati presenti in letteratura, inclusi quelli provenienti da registri o istituti di controllo nazionali, non sono del tutto comparabili e mostrano alcune discordanze2,3,4. È quindi difficile, se non impossibile, fornire in poche righe dati precisi ed esaustivi sulle cause di revisione delle diverse protesi di spalla. A scopo riassuntivo, in Tabella I sono riportate le principali indicazioni per gli interventi di revisione, senza entrare nel dettaglio sulle possibili procedure adottabili.
Per quanto riguarda le protesi anatomiche, merita di essere evidenziato un confronto tra protesi parziali e totali. Vi sono numerose evidenze cliniche a supporto della superiorità delle protesi totali negli outcome primari5, poiché l’impianto della sola componente omerale è gravato da un’elevata percentuale di esiti dolorosi per problematiche glenoidee, denominate in vario modo (usura, glenoidite, iperpressione, ecc). Per questo motivo e per il miglioramento dei materiali, del design e delle tecniche di impianto della componente glenoidea, che consentono aspettative di sopravvivenza ben superiori rispetto al passato, le protesi totali sono oggi la scelta di gran lunga preferita per la protesizzazione anatomica della spalla. Va inoltre sottolineato che la revisione di una protesi parziale non offre prospettive di risultati clinico-funzionali migliori rispetto alle revisioni di artroprotesi, nonostante l’assenza della componente glenoidea possa apparire come un vantaggio anatomico per l’impianto scapolare6.
L’esperienza maturata negli anni con la protesi inversa, unitamente al progresso tecnico-scientifico, ha modificato l’incidenza delle cause di revisione per questi impianti. Il problema dell’incisura (notching) glenoidea inferiore, la cui comparsa e progressione era quasi costante con il primo modello di Grammont, è stato del tutto ridimensionato nell’ultimo decennio7. Questo ha portato a una netta riduzione delle mobilizzazioni della componente glenoidea e attualmente sono l’instabilità e l’infezione a rappresentare le principali cause di revisione delle protesi inverse.
REVISIONE DELLA COMPONENTE OMERALE
La possibilità di utilizzare una protesi anatomica, sia essa parziale o totale, per un intervento di revisione è subordinata alla integrità (almeno parziale) anatomo-funzionale della cuffia. L’assenza del tendine sottoscapolare è una controindicazione assoluta a questo tipo di impianto, fatta eccezione per interventi di “salvataggio”, nei quali la sua unica finalità è quella di preservare lo spazio occupato dall’omero.
In presenza di difetti ossei o di rilevanti sovvertimenti strutturali dell’omero prossimale che coinvolgano le tuberosità, un recupero funzionale più o meno soddisfacente della spalla risulta possibile solo attraverso l’impiego di una protesi inversa.
Bisogna tuttavia ricordare che la rotazione esterna dell’articolazione gleno-omerale è assicurata solo dai muscoli posteriori della cuffia (sottospinoso e piccolo rotondo) e che la mobilità articolare viene notevolmente compromessa qualora la loro azione sull’omero prossimale venga a mancare. Per questo motivo, pur non essendone prerogativa, la ricostruzione del trochite o la reinserzione dei tendini extrarotatori deve essere sempre considerata e ricercata in un intervento di revisione.
Qualora la perdita di tessuto osseo, preesistente o conseguente all’intervento di revisione, si estenda al di sotto dell’inserzione del muscolo deltoide, le possibilità di successo terapeutico con una protesi inversa si riducono in modo drastico, con un aumento significativo del rischio di complicanze, prima tra tutte l’instabilità.
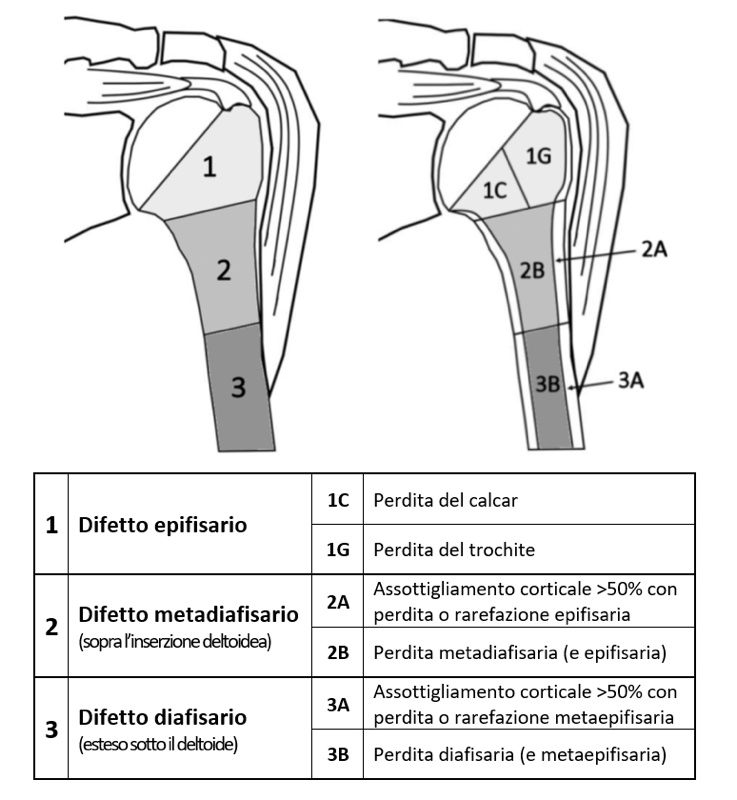
Il sistema PHAROS (Proximal Humeral Arthroplasty Revision Osseous inSufficiency) è stato recentemente introdotto per classificare i difetti ossei dell’omero prossimale al fine di agevolare la pianificazione preoperatoria negli interventi di revisione (Fig. 1). Sebbene la sua validità, affidabilità e riproducibilità nella pratica clinica non siano state ancora comprovate, questo sistema rappresenta un punto di partenza per la pianificazione della revisione della componente omerale e la definizione di algoritmi terapeutici 8. La progressiva estensione del deficit di bone stock si associa inizialmente (tipo 1-2) a una compromissione anatomo-funzionale della cuffia, per poi causare la perdita dell’azione del deltoide e marcate difficoltà nella fissazione dello stelo (tipo 3). La crescente esperienza in questo campo si gioverà quindi di sistemi classificativi come il PHAROS per migliorare la ricerca clinica, favorire la comparazione di dati e promuovere lo sviluppo di soluzioni innovative per queste condizioni di difficile approccio.
REVISIONE DELLA COMPONENTE GLENOIDEA
L’usura e la mobilizzazione della glena sono state per anni una delle principali cause di revisione delle protesi totali di spalla. Negli impianti anatomici la componente glenoidea è sempre stata considerata l’anello debole del sistema, non garantendo sopravvivenze paragonabili a quelle della componente omerale. Allo stesso modo, nella protesi inversa di Grammont, il fenomeno del notching scapolare metteva a rischio a breve e medio termine la fissazione della metaglena, rappresentando una causa frequente di fallimento per questi impianti. Questo ha fatto sì che l’esperienza maturata in questo campo sia maggiore rispetto a quella sviluppata per la revisione della componente omerale.
Va tenuto presente che molti, forse la maggior parte, dei fallimenti della glena protesica sono paucisintomatici. Per questo motivo, soprattutto nei pazienti anziani, non si ricorre necessariamente al trattamento chirurgico, in particolare se la bassa espressività clinica della condizione non si associa a un danno anatomico rilevante o progressivo.
La mobilizzazione di una componente glenoidea anatomica può essere trattata con la semplice trasformazione in una protesi parziale (con eventuale adattamento dimensionale della testa omerale per compensare lo spessore mancante) se la cuffia dei rotatori è ancora conservata. Tuttavia è molto più frequente la sua revisione con l’impianto di una protesi inversa, anche perché il metal back delle metaglene garantisce soluzioni di fissazione nettamente superiori a quelle ottenibili con gli impianti anatomici. I sistemi modulari di ultima generazione consentono di lasciare in sede lo stelo diafisario, sostituendo solo la parte epifisaria della componente omerale, oltre naturalmente alla glena. Questo rappresenta un vantaggio in presenza di steli osteointegrati o cementati, specie in pazienti con corticali diafisarie assottigliate, dove la rimozione dello stelo si traduce in procedure più invasive, problematiche chirurgiche maggiori e outcome clinici peggiori.
La definizione del deficit di bone stock della glena e del collo scapolare è un aspetto essenziale per la pianificazione di un intervento di revisione glenoidea e per verificarne la fattibilità. Le tecniche di visualizzazione e stampa tridimensionale hanno migliorato in modo significativo lo studio anatomico preoperatorio, permettendo nel contempo di sviluppare tecniche chirurgiche (navigazione, robotica) e impianti customizzati atti ad affrontare situazioni di difficile risoluzione con le metodiche tradizionali. Va sempre tenuto presente che negli interventi di revisione glenoidea si lavora su piccole quantità di tessuto osseo, dove una fissazione affidabile della componente può essere un obiettivo troppo ambizioso in presenza di osteolisi estese. È quindi sempre bene ricordare che la semplice rimozione della protesi glenoidea, associata a uno “spaziatore” omerale, può rappresentare la soluzione più conveniente per molti pazienti.
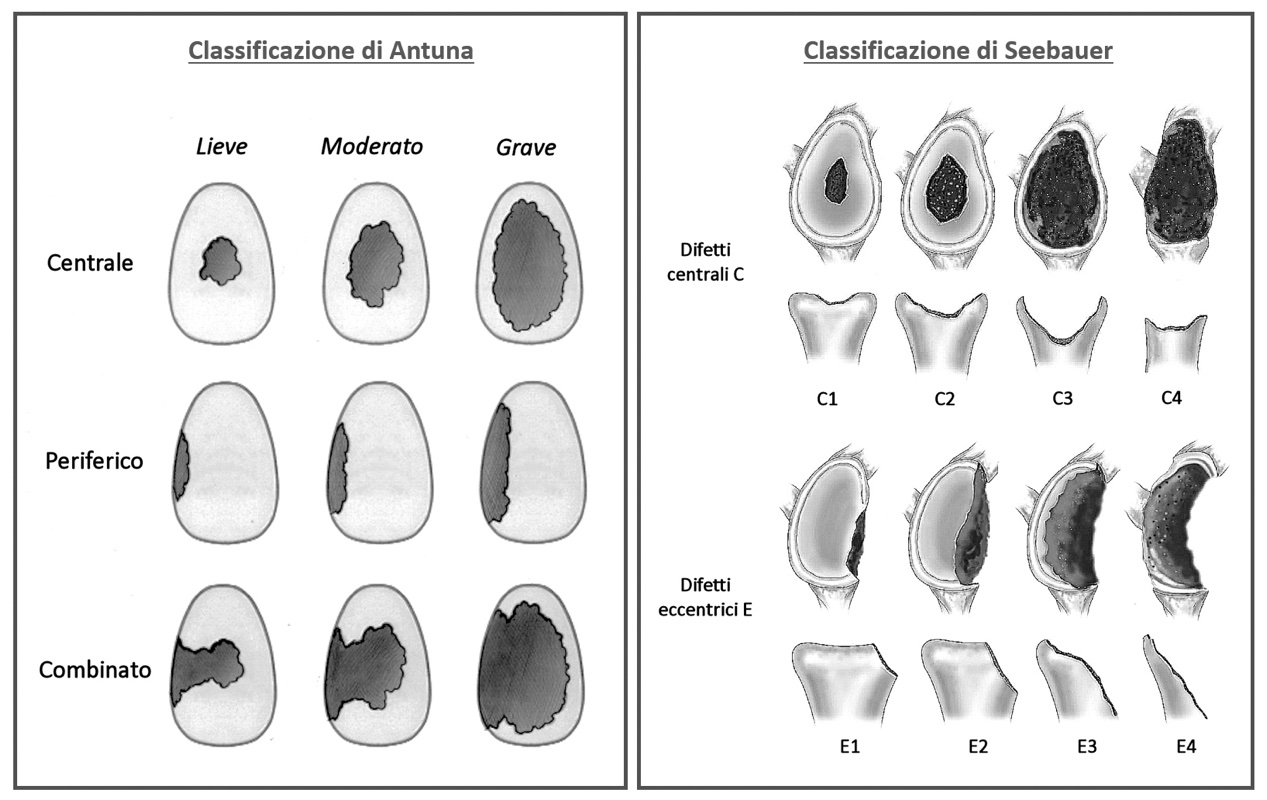
Tra le classificazioni dei difetti ossei glenoidei, quella di Antuna è forse quella più utilizzata, anche perché descritta nel 20019. Più di recente, Seebauer ha proposto un sistema classificativo dove il deficit di bone stock viene definito nei due piani, orizzontale e verticale, fornendo una più precisa rappresentazione tridimensionale dell’osteolisi scapolare (Fig. 2)10.
Le tecniche di revisione della componente glenoidea comportano molto spesso l’impiego di innesti o sostituti ossei, in forma morcellizzata per il riempimento di difetti contenuti o in forma strutturata per la ricostruzione di difetti segmentali più o meno estesi. La possibilità di fissazione con viti, offerta dalle componenti con metal back, è una caratteristica indispensabile per ottenere una stabilità primaria affidabile dell’impianto. Anche per questo motivo l’impego di protesi inverse ha quasi del tutto soppiantato quello delle protesi anatomiche negli interventi di revisione protesica di questo distretto anatomico.
CAPITOLO 40Bibliografia.
- Wagner ER, Chang MJ, Welp KM, et al. The impact of the reverse prosthesis on revision shoulder arthroplasty: analysis of a high-volume shoulder practice. J Shoulder Elbow Surg 2019 Feb; 28:e49-e56. .
- Bohsali KI, Bois AJ, Wirth MA. Complications of shoulder arthroplasty. J Bone Joint Surg Am 2017 Feb 1; (3):256-269. doi: 10.2106/JBJS.16.00935 .
- Gauci MO, Cavalier M, Gonzalez JF, et al. Revision of failed shoulder arthroplasty: epidemiology, etiology, and surgical options. Shoulder Elbow Surg. 2020 Mar;29(3):541-549. doi: 10.1016/j.jse.2019.07.034.
- Weatherby PJ, Efejuku TA, Somerson JS. Complications after anatomic shoulder arthroplasty: revisiting leading causes of failure. Orthop Clin North Am. 2021 Jul;52(3):269-277. doi: 10.1016/j.ocl.2021.03.002.
- Singh Jagdev B, McGrath J, Cole A et al. Total shoulder arthroplasty vs. hemiarthroplasty in patients with primary glenohumeral arthritis with intact rotator cuff: meta-analysis using the ratio of means. J Shoulder Elbow Sur. 2022 Dec;31(12):2657-2670. doi: 10.1016/j.jse.2022.07.012.
- Sheth MM, Sholder D, Getz CL et al. Revision of failed hemiarthroplasty and anatomic total shoulder arthroplasty to reverse total shoulder arthroplasty. J Shoulder Elbow Surg. 2019 Jun;28(6):1074-1081. doi: 10.1016/j.jse.2018.10.026.
- Alberio RL, Landrino M, Fornara P, et al. Short-term outcomes of the Grammont reverse shoulder arthroplasty: comparison between first and second generation Delta prosthesis. Joints. 2021 Jun 20;7(4):141-147. doi: 10.1055/s-0041-1731010.
- Chalmers PN, Romeo AA, Nicholson GP, et al. Humeral bone loss in revision total shoulder arthroplasty: the Proximal Humeral Arthroplasty Revision Osseous inSufficiency (PHAROS) classification system. Clin Orthop Relat Res. 201 Feb;477(2):432-441. doi: 10.1097/CORR.0000000000000590.
- Antuna SA, Sperling JW, Cofield RH, et al. Glenoid revision surgery after total shoulder arthroplasty. J Shoulder Elbow Surg. 2001 May-Jun;10(3):217-24. doi: 10.1067/mse.2001.113961.
- Gupta A, Thussbas C, Koch M, et al. Management of glenoid bone defects with reverse shoulder arthroplasty-surgical technique and clinical outcomes. J Shoulder Elbow Surg. May;27(5):853-862. doi: 10.1016/j.jse.2017.10.004