Malattia Di Legg-Calvé-Perthes
Dipartimento di Chirurgia Generale e Specialità Medico-Chirurgiche, Sezione di Ortopedia e Traumatologia, P.O. “Policlinico Gaspare Rodolico”, Università degli Studi di Catania, Catania
DEFINIZIONE
Per malattia di Legg-Calvè-Perthes si intende una necrosi avascolare idiopatica della testa femorale con interruzione dell’apporto ematico alla stessa che può portare a una deformità progressiva e maggiore probabilità di sviluppare un’artrosi precoce secondaria 1. È stata descritta simultaneamente per la prima volta nel 1910 da Arthur Legg, Jacques Calvé e George Perthes.
EPIDEMIOLOGIA
Diagnosticata prevalentemente in età compresa tra i 3 e i 12 anni, presenta un picco di incidenza tra i 5 e i 7 anni. Le regioni equatoriali hanno bassa incidenza di malattia, il Nord Europa ha la più alta incidenza documentata con un rapporto Maschi/Femmine di 3-5/1. È stato descritto un interessamento di entrambe le teste femorali nel 10-24%, dei casi, con familiarità nell’8-12% dei casi 2.
EZIOLOGIA
Ad oggi non esiste un consenso comune su quali siano i fattori a influenzare l’insorgenza della patologia. L’opinione prevalente è che ci sia di base una multifattorialità in cui, su un substrato genetico, agiscano fattori ambientali scatenanti. Sono stati in letteratura identificati diversi casi di malattia in soggetti appartenenti allo stesso nucleo familiare associati a mutazioni del gene del collagene di tipo 2 (COL2A1). Tra i fattori ambientali sembrerebbe che l’esposizione al fumo, peri-partum o post-partum, sia associato a un più alto rischio di sviluppare la malattia. Altri fattori annessi all’insorgenza potrebbero essere un basso livello socio-economico, trauma maggiore e microtraumatismi ripetuti, basso peso alla nascita, sindrome da deficit di attenzione e iperattività, obesità e maggiori livelli ematici di leptina, polimorfismo dei geni che codificano per il fattore V di Leiden e per la protrombina II, bassi livelli sierici di VEGF, IGF-1 e proteina legante IGFBP-3, polimorfismi per le citochine proinfiammatorie e aumento dei lori livelli, principalmente IL-6, e maggiori livelli di proteine pro-apoptotiche, su tutte le Ba x1. Di recente è emerso che un sinergismo tra condizione ischemica, immaturità scheletrica e biomeccanica alterata concorra alla insorgenza della patologia 3, inoltre un ritardo nell’ossificazione endocondrale dell’epifisi femorale potrebbe avere un ruolo non secondario 4.
ANATOMIA PATOLOGICA
I principali cambiamenti istopatologici rilevati su campioni anatomici sono:
- presenza di zone ossee ischemiche con osteociti con nuclei assenti o picnotici;
- capsula ispessita ed edematosa per proliferazione condrocitaria;
- sinovia iperplasica e iperemica, ricca di villi, con infiltrati istiocitari e linfoplasmacellulari;
- strati superficiale e medio della cartilagine articolare indenni, estesa necrosi condrocitaria nello stato profondo;
- presenza di frattura subcondrale;
- cartilagine di accrescimento irregolare e interrotta con colonne di cartilaginee che spesso si estendono alla regione metafisaria adiacente che radiograficamente appaiono come zone di radiotrasparenza;
- formazioni cistiche piene di liquido a livello metafisario;
- neoproduzione di tessuto osseo nella fase riparativa.
- Le alterazioni sopraelencate sono più o meno riscontrabili in relazione alle varie fasi di malattia 5.
CLASSIFICAZIONI
Sono state proposte varie metodiche classificative 5, una delle più accettate è quella proposta da Herring, basata sul grado di collasso del pilastro laterale (utile nella scelta iniziale del trattamento):
-
Gruppo A: pilastro laterale integro;
-
Gruppo B: collasso del pilastro laterale < 50%;
-
Gruppo B/C: collasso del pilastro laterale pari circa al 50%;
-
Gruppo C: collasso del pilastro laterale > 50%.
Altre classificazioni ampiamente utilizzate sono:
-
Salter-Thompson, basata sulla estensione e localizzazione della frattura sub-condrale:
-
GRUPPO A: < 50% dell’epifisi interessata;
-
GRUPPO B: > 50% dell’epifisi interessata.
-
Catteral, basata sulla distribuzione geografica della necrosi ossea epifisaria:
-
GRUPPO I:
-
interessamento < 25% della porzione anteriore del nucleo;
-
assenza di collasso, sequestri e di reazione metafisaria.
-
GRUPPO II:
-
interessamento del 50-70% della porzione anteriore del nucleo;
-
pilastro laterale e mediale intatti, presenza di lieve reazione metafisaria.
-
GRUPPO III:
-
interessamento massivo del nucleo a eccezione di una porzione mediale;
-
interessamento del pilastro laterale, presenza di collassi e sequestri, reazione metafisaria diffusa.
-
GRUPPO IV:
-
interessamento completo della testa femorale;
-
interessamento del pilastro laterale e mediale, reazione metafisaria massiva.
-
Stulberg, basata sulla deformità residua della testa femorale (utile nella valutazione prognostica):
-
I TIPO: anca normale;
-
II TIPO: testa buona, acetabolo congruente;
-
III TIPO: testa discreta (a fungo), acetabolo congruente;
-
IV TIPO: testa mediocre (appiattita), acetabolo congruente;
-
V TIPO: testa mediocre (appiattita), acetabolo incogruente.
DIAGNOSI
L’approccio diagnostico prevede un’attenta raccolta anamnestica al fine di ricercare un singolo evento traumatico o ripetuti, bassa statura, iperattività, unitamente a un accurato esame clinico. All’esame obiettivo: i pazienti si presentano spesso con zoppia, antalgica o da Trendelenburg, dolore, solitamente localizzato all’inguine o in regione trocanterica. Spesso può essere riferito in regione anteriore di coscia o in corrispondenza del ginocchio (falsando la diagnosi) e può aggravarsi durante l’attività fisica. Tali sintomi tendono ad alleviarsi col riposo o con l’assunzione di FANS. Nelle fasi inziali il paziente avrà una contrattura in flessione dell’anca, con limitazione dell’abduzione e della rotazione interna. Col progredire del tempo può presentarsi una contrattura antalgica degli adduttori. Nelle fasi ancora più avanzate possono svilupparsi lesioni osteocondrali e fenomeni di impingement con segni di artrosi secondaria precoce (Tab. I) 6.
Le indagini strumentali sono fondamentali per confermare la diagnosi. L’esame principe è ancor oggi la radiografia con le due proiezioni standard.Waldenstrom descrisse per la prima volta nel 1922 quattro stadi radiografici connessi alla patologi a6 (Tab. II).
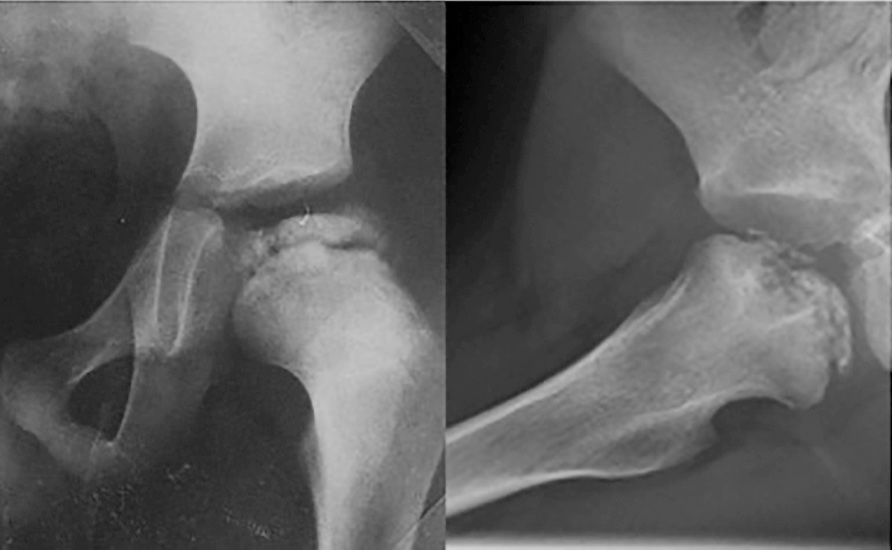
Le proiezioni da eseguire in caso di sospetto sono l’anteroposteriore e la frog-lateral d’anca (Fig. 1). In base alle manifestazioni radiografiche è possibile classificare la malattia sulla base dell’estensione e della gravità e distinguere due fasi: attiva, quando l’epifisi femorale appare sclerotica con o senza presenza di collasso e fenomeni di riossificazione, di guarigione, quando nessun residuo osseo avascolare può essere radiologicamente identificato 5.
Oltre all’approccio radiografico sono previste diverse tecniche di imaging.
L’Ecografia, di facile esecuzione e basso costo, solitamente mostra la presenza di versamento che, se persistente, deve indurre al sospetto di malattia. Non è specifica per patologia, ma aiuta a differenziare le fasi iniziali dal quadro di sinovite transitoria dell’anca. Nei pazienti con sinovite la distensione capsulare è attribuibile al versamento, nei pazienti con Malattia di Perthes a ispessimento della membrana sinoviale 6. Fornisce informazioni utili su copertura acetabolare della testa femorale e appiattimento o alterazioni di forma della testa femorale.
La Risonanza Magnetica Nucleare è estremamente utile nell’identificazione precoce dell’estensione della necrosi epifisaria e dell’interessamento della cartilagine di accrescimento e della metafisi. Fornisce informazioni sulla morfologia della testa femorale e dell’acetabolo, sul grado di estrusione della testa femorale e sull’entità di dislocazione supero-laterale della testa femorale (sublussazione) 5.
La Scintigrafia è una metodica poco utilizzata. Conway 5 descrisse un sistema classificativo con significato prognostico che precede le alterazioni radiografiche di tre mesi. Questa classificazione si basa su modelli scintigrafici indicativi di rivascolarizzazione e ricanalizzazione dei vasi e prevede tre gruppi A, B, C di significato prognostico decrescente. Utile nella valutazione precoce dei pazienti affetti da malattia 5.
L’Artrografia viene utilizzata per valutare le possibili opzioni di trattamento. Deve essere eseguita in sala operatoria in condizioni di estrema sterilità. Nelle fasi iniziali potrebbe non mostrare alterazioni o mostrare solo un lieve appiattimento della testa femorale. Permette di valutare l’entità della copertura della testa femorale e i ROM dell’anca direttamente in fluoroscopia 5.
La Tomografia Computerizzata consente una diagnosi precoce di collasso osseo e dei sottili cambiamenti nel pattern trabecolare osseo. Nelle fasi avanzate permette di identificare la presenza di cisti intraossee. Fornisce lo studio tridimensionale della testa femorale e del suo rapporto con l’acetabolo. Le alti dosi di radiazioni utilizzate ne limitano fortemente l’utilizzo 5.
TRATTAMENTO
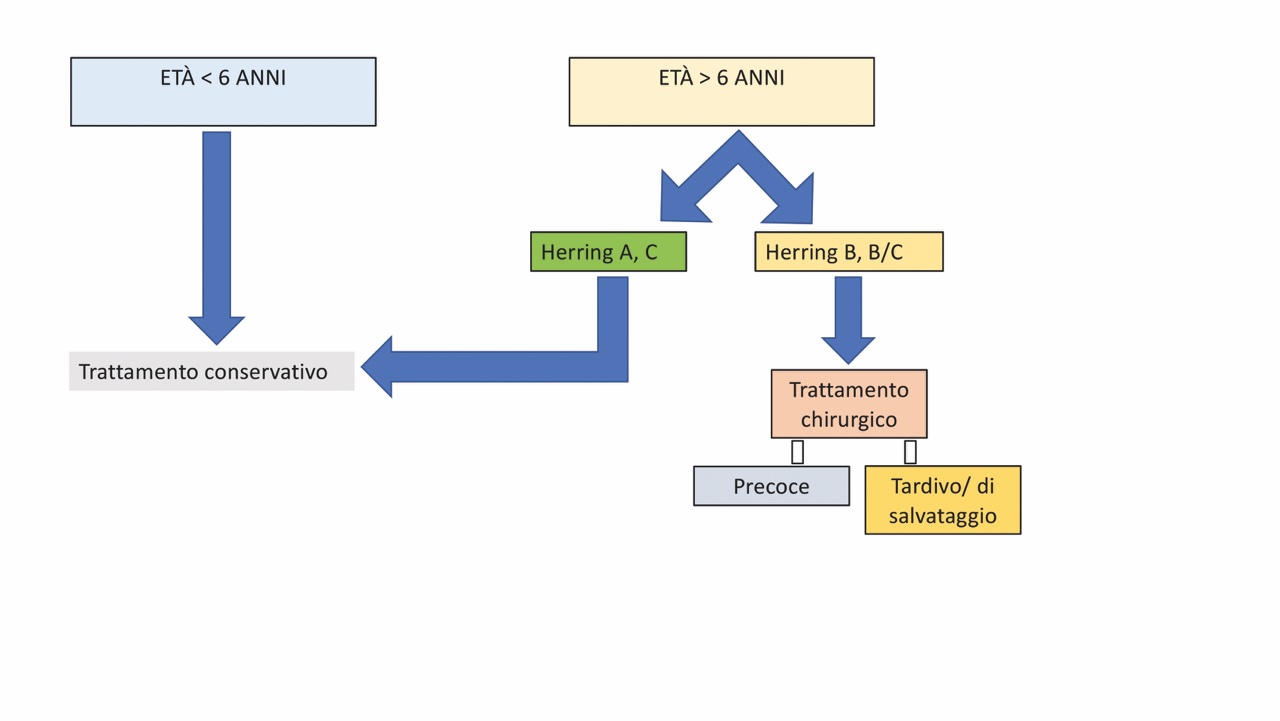
Il trattamento è ad oggi privo di linee guida ufficiali: l’età inziale di insorgenza di malattia e la gravità radiografica iniziale, principalmente in accordo alla classificazione di Herring, ne guidano la scelta. Esiste tuttavia una tendenza comune che prevede la scelta del trattamento conservativo nei pazienti di età inferiore ai 6 anni e nei pazienti di età superiore ai 6 anni con anche di tipo Herring A e C, oltre che nei casi a esordio tardivo (Fig. 2) 6.
Il trattamento, sia esso conservativo che chirurgico, mira al concetto biomeccanico del “Contenimento” secondo il quale la testa femorale deve perfettamente essere contenuta all’interno dell’acetabolo, favorendone così il suo corretto modellamento e prevenendo le possibili deformità 6.
Il trattamento conservativo “sintomatico” include carico protetto, terapia medica con FANS e terapia fisica volta al recupero della totale articolarità dell’anca, con particolare attenzione all’abduzione, quello “contenitivo” prevede l’utilizzo di tutori in abduzione o apparecchi gessati di Petrie, ad oggi in disuso6.
Il trattamento chirurgico prevede varie opzioni in base alle diverse indicazioni. Le fasi di malattia ottimali, secondo classificazione di Waldenstrom, in cui intervenire chirurgicamente sono l’iniziale e la fase precoce dello stadio di frammentazione. Requisito fondamentale per un buon outcome chirurgico è il recupero ottimale dell’articolarità dell’anca, obiettivo perseguibile anche con l’utilizzo di una trazione gentile preoperatoria 6.
L’osteotomia femorale varizzante (FVO) e l’osteotomia innominata di Salter sono tra le tecniche chirurgiche più utilizzate nelle fasi precoci della malattia.
L’osteotomia femorale varizzante trova impiego nei bambini di età superiore ai 6 anni con interessamento > del 50% dell’epifisi femorale, gli angoli di varizzazione consigliati sono 10-15°, complicanze post-operatorie riscontrabili sono l’eccesivo varismo indotto, accorciamento dell’arto e zoppia 6.
L’osteotomia innominata di Salter fu la prima osteotomia di reindirizzamento pelvico a essere utilizzata nel 1962 con indicazioni e risultati sovrapponibili alla FVO; le principali complicanze riscontrate connesse alla tecnica sono l’allungamento dell’arto e la diminuzione dei gradi di flessione dell’anca 6. La combinazione di entrambe le tecniche viene utilizzata quando una sola di queste due procedure non è sufficiente a garantire il principio cardine del contenimento, condizione associata a casi a esordio tardivo e con grave coinvolgimento della testa femorale 7.
L’artrodiatasi e l’osteotomia di rotazione trans-trocanterica rappresentano approcci chirurgici alternativi alla patologia 6. Il primo prevede l’utilizzo di un fissatore esterno in distrazione e consente il contenimento della testa femorale all’interno dell’acetabolo senza indurre stress meccanico. Lo scopo di tale trattamento è ripristinare l’articolarità dell’anca evitando il contatto tra testa femorale e acetabolo favorendo così la rigenerazione e la riparazione della cartilagine articolare danneggiata. Ad oggi trova poco impiego in ambito chirurgico poiché di difficile gestione e con risultati non superiori rispetto ad altre tecniche. Il secondo, volto a modificare le zone di carico, trova indicazione nei casi a esordio tardivo, età > 9 anni.
Tra le tecniche di salvataggio ricordiamo l’osteotomia di Chiari, oggi poco utilizzata e confinata solamente ai casi di grave entità, l’acetaboloplastica a scaffale e l’osteotomia tripla innominata 6. Le complicanze chirurgiche sono principalmente connesse al tipo di tecnica utilizzata, ma ricordiamo che la necrosi avascolare iatrogena è la più temibile 6.
OUTCOME CHIRUGICO A LUNGO TERMINE
Il trattamento chirurgico nei pazienti di età superiore ai 6 anni con anche Herring B, B/C ha un ottimo outcome con alte percentuali di anche Stulberg I e II, a differenza delle anche di tipo C, con marcate percentuali di Stulberg III e IV 7.
TRATTAMENTO DELLE COMPLICANZE
I pazienti con deformità residua della testa femorale e alterazioni acetabolari sono suscettibili allo sviluppo di coxalgia persistente. Possibili complicanze riscontrabili sono il conflitto femoro-acetabolare (FAI), che trova indicazione chirurgica quando il dolore è persistente nonostante il trattamento conservativo, hinge abduction, coxa magna, coxa brevis e coxa irregularis che dovranno essere trattate con idonee procedure chirurgiche 6.
Infine, la possibilità di dover ricorrere a una sostituzione protesica per coxartrosi precoce, under 50 anni, è solo del 7% nei casi chirurgici con range più elevati, 24-40%, nei pazienti trattati conservativamente 7.
CAPITOLO 13Bibliografia.
-
Pavone V, Chisari E, Vescio A, et al. Aetiology of Legg-Calvé-Perthes disease: A systematic review. World J Orthop. 2019 Mar 18;10(3):145-165. doi: 10.5312/wjo.v10.i3.145.
-
Perry DC, Machin DMG, Pope D, et al. Racial and Geographic Factors in the Incidence of Legg-Calvé-Perthes’ Disease: A Systematic Review. Am J Epidemiol. 2012 Feb 1;175(3):159-66. doi: 10.1093/aje/kwr293.
-
Pinheiro M, Dobson, CA, Perry D, et al. New insights into the biomechanics of Legg-Calvé-Perthes’ disease: The Role of Epiphyseal Skeletal Immaturity in Vascular Obstruction. Bone Joint Res. 2018 Feb;7(2):148-156. doi: 10.1302/2046-3758.72.BJR-2017-0191.R1.
-
Kitoh H, Kitakoji T, Katoh M, et al. Delayed ossification of the proximal capital femoral epiphysis in Legg-Calvé-Perthes’ disease. J Bone Joint Surg Br. 2003 Jan;85(1):121-4. doi: 10.1302/0301-620x.85b1.13426.
-
Dimeglio A, Canavese F. Imaging in Legg-Calvé-Perthes Disease. Orthop Clin North Am. 2011 Jul;42(3):297-302, v. doi: 10.1016/j.ocl.2011.04.003.
-
Herring JA. Tachdjian’s Pediatric Orthopaedics. Elsevier – Saunders 2019, pp. 2043.
-
Caldaci A, Testa G, Dell’Agli E, et al. Mid–Long-Term Outcomes of Surgical Treatment of Legg-Calvè-Perthes Disease: A Systematic Review. Children (Basel). 2022 Jul 27;9(8):1121. doi: 10.3390/children9081121.