Spalla: patologia degenerativa e sostituzione protesica
Dipartimento di Scienze Anatomiche, Istologiche, Medico-legali e dell’Apparato Locomotore, Sapienza Università di Roma; Ospedale Umberto I, Roma
La prevalenza dell’artrosi della spalla è assai inferiore rispetto a quella dell’anca e del ginocchio1. Pertanto, è ragionevole pensare che l’assenza del carico preservi l’articolazione da una precoce usura della cartilagine articolare. Raramente l’artrosi della spalla insorge prima della sesta decade di vita; tuttavia, nei casi di artrosi giovanile è frequente rilevare una predisposizione genetica. Sono considerate cause predisponenti all’artrosi: le fratture della testa omerale con split della superficie articolare e le lussazioni recidivanti; inoltre vengono considerate fattori di rischio malattie reumatiche, pseudotumorali, ematologiche e dismetaboliche poiché causano un’infiammazione cronica del microambiente articolare; per i possibili conseguenti disturbi del microcircolo periferico o per l’assunzione dei farmaci impiegati per gestirle.
Nella pratica comune si distinguono due tipi di artrosi della spalla: la concentrica e l’eccentrica2,3. La prima, per lo più idiopatica, è caratterizzata radiograficamente dai classici elementi dell’artrosi: riduzione dello spazio articolare; sclerosi dell’osso subcondrale; formazione di osteofiti (antero o postero inferiori) e di cavità geodiche. La testa omerale è spesso appiattita. L’artrosi eccentrica può avere tutti i suddetti elementi, ma si differenzia dall’altra per la migrazione prossimale della testa dell’omero causata dalla rottura massiva della cuffia dei rotatori (artropatia da cuffia). A questi tendini, infatti, viene attribuito il ruolo di stabilizzatori dinamici dell’articolazione e di centratori della testa dell’omero nella cavità glenoidea. La risalita della testa dell’omero potrebbe facilitare una erosione della porzione superiore della superficie articolare glenoidea e del margine antero-inferiore dell’acromion. Inoltre, la migrazione prossimale della testa dell’omero causa una instabilità articolare e una usura precoce delle aree articolari sovraccaricate. Secondo la teoria “nutrizionale” il danno cartilagineo avverrebbe perché in assenza della cuffia il liquido sinoviale si disperderebbe anziché essere concentrato nell’ambiente articolare. La scarsa concentrazione di liquido sinoviale e la ridotta mobilità della spalla ostacolerebbero il meccanismo di diffusione del liquido sinoviale nella cartilagine. L’artropatia da cuffia è stata considerate anche una malattia reumatica autoimmune. Così come il lupus eritematoso sistemico (LES) o la sclerodermia i pazienti con artropatia da cuffia sono spesso di sesso femminile. Nessuno studio ha però confermato questa ipotesi. Un nostro studio ha anche escluso la possibilità che i giovani iperlassi possano avere più possibilità di sviluppare un’artropatia di cuffia rispetto a un gruppo di controllo.
QUADRO CLINICO
Generalmente, i pazienti con artrosi della spalla hanno più di 65 anni. Essi riferiscono di avere dolore, ma raramente l’intensità è marcata. Sono spesso donne con sintomi di lunga durata. Il braccio dominante è quello più frequentemente coinvolto. Usualmente, il dolore è distribuito sulla regione antero-laterale della spalla, raramente si estende alla base del collo, non oltrepassa il gomito, non si irradia alla regione scapolare, non si accompagna a parestesie, disturba il sonno e si intensifica con le attività quotidiane. Molti pazienti riferiscono di avvertire scrosci endoarticolari. Quando questi sono presenti, sono facilmente evocabili con il test di Jobe o con il full can test1,4. Nei pazienti magri è talvolta visibile una deformità del profilo della spalla, soprattutto nei pazienti con artropatia della cuffia a motivo della risalita della testa dell’omero. Occasionalmente la spalla è tumefatta, per la presenza di abbondante liquido sinoviale. L’atrofia della loggia sopra e sottospinosa è sempre osservabile nei pazienti con artropatia da cuffia, ma occasionalmente anche in quelli con artropatia concentrica a motivo del non uso dei muscoli del cingolo scapolare.
La mobilità attiva e passiva della spalla è limitata per la deformità scheletrica, per la contrattura dei tessuti molli e per la instabilità statica gleno-omerale.
Test funzionali (ASES e SST) indicano che i pazienti con artropatia da cuffia raggiungono punteggi più bassi (peggiori) rispetto a quelli con artropatia concentrica. Ciò perché i pazienti con artropatia da cuffia sono generalmente più anziani; perché la riduzione della mobilità è più accentuata rispetto agli altri artrosici e perché hanno costantemente un deficit di forza in extrarotazione che contribuisce a limitare le comuni attività quotidiane.
INDICAZIONE ALL’IMPIANTO DI UNA PROTESI
L’impianto di una protesi è consigliabile in pazienti con artropatia concentrica od eccentrica della spalla responsabile di dolore e riduzione della mobilità. Spesso questi due elementi possono compromettere l’espletamento delle attività quotidiane e minare lo stato di autonomia del paziente (soprattutto se molto anziano). Inoltre, occorre che il paziente non abbia risposto adeguatamente al trattamento conservativo; che sia motivato a intraprendere un lungo percorso riabilitativo (con il fisioterapista e autonomamente) e che non vi siano comorbidità che controindichino il trattamento chirurgico.
PIANIFICAZIONE PRE-OPERATORIA
L’esame obiettivo e quello radiografico sono già dirimenti per formulare una diagnosi di artropatia della spalla, ma esami di secondo livello (RM e TC) consentono di stabilire la condizione della cuffia dei rotatori (integrità; spessore; stato di degenerazione) e le caratteristiche scheletriche dell’omero e della glena. L’esame TC è indispensabile per quantificare una possibile usura glenoidea e classificarla. Ciò fornirà all’operatore informazioni se la versione glenoidea deve essere ripristinata. Negli ultimi anni sono stati elaborati software di simulazione e strumenti preoperatori in grado di fornire al chirurgo un planning dettagliato riguardo le taglie e il corretto posizionamento delle componenti protesiche, sia glenoidea che omerale; tale planning, dopo essere stato visionato e perfezionato dall’operatore potrà essere fedelmente riprodotto grazie all’utilizzo di strumenti innovativi come la navigazione e la realtà aumentata intraoperatoria che permettono di raggiungere una precisione chirurgica elevatissima.
Ci sono due grandi famiglie di protesi: le anatomiche e le inverse5,6. Le prime sono indicate per pazienti relativamente giovani, con artropatia concentrica e riproducono l’anatomia originaria. Le inverse sono indicate per i pazienti molto anziani, a prescindere dal tipo di artropatia, e per tutti quelli con artropatia da cuffia. Ideata negli anni 80’ da Paul Grammont, questa protesi inverte, rispetto alla normalità, le superfici articolari proponendo al chirurgo l’impianto di una glenosfera e di una coppa omerale. Questa nuova situazione ha la peculiarità di incrementare il braccio di leva del deltoide (coinvolgendo i fasci anteriori, laterali e posteriori) e di esaltare la mobilità attiva ottenibile dal paziente privo della cuffia dei rotatori. Inoltre, la protesi inversa trasforma le forze di taglio intorno alla spalla in forze compressive creando un momento rotazionale favorente l’azione del deltoide. L’aumento della superficie articolare incrementa la stabilità articolare e potenzia il range di movimento.
Le protesi attualmente in commercio sono modulari ossia costituite da singole porzioni tra loro assemblabili. Fanno accezione alcune protesi tumorali impiantate nelle grandi resezioni che conservano una struttura monoblocco. Inoltre, le protesi vengono proposte nella versione a stelo lungo, corto o senza stelo: ognuna delle quali ha precise indicazioni.
PROTESI ANATOMICA
Eseguendo una resezione omerale al collo anatomico e utilizzando un impianto ideato per ripristinare la retroversione, inclinazione, l’offset mediale e posteriore della testa originale e una profondità identica a quella della testa omerale nativa, i singoli bracci di leva dei muscoli della cuffia dei rotatori vengono ripristinati. La componente cefalica è disponibile in diverse taglie e spessori e può essere impiantata anche in maniera eccentrica. Due filosofie di pensiero, riguardo alle caratteristiche della componente glenoidea, hanno diviso negli anni i chirurghi di spalla. La prima soluzione prevede di impiantare componenti glenoidee in polietilene con chiglia o pegs. Queste componenti vengono sempre cementate. L’altra possibilità e di impiantare una componente glenoidea costituita da un metal back curvilineo, che si avvita alla superficie cruentata della glena, e una componente in polietilene a incastro sulla superficie accogliente del metal back. I fautori del polietilene cementato hanno giustificato la loro scelta ritenendo che con il metal back vi fosse un’alta percentuale di dissociazione e usura delle componenti e rottura delle viti e un eccessivo spessore del complesso metal back + polietilene. In realtà ciò poteva essere vero con metal back di vecchia generazione, con profilo piatto e con sistemi di fissazione discutibili. Nel caso di deficit ossei glenoidei in grado di modificare la fisiologica versione, le aziende forniscono glene con cunei di correzione. Tuttavia, quest’ultima può essere ottenuta anche effettuando un “reaming eccentrico” della superficie glenoidea o interponendo un cuneo osseo ricavato dalla testa omerale asportata e appropriatamente modellato.
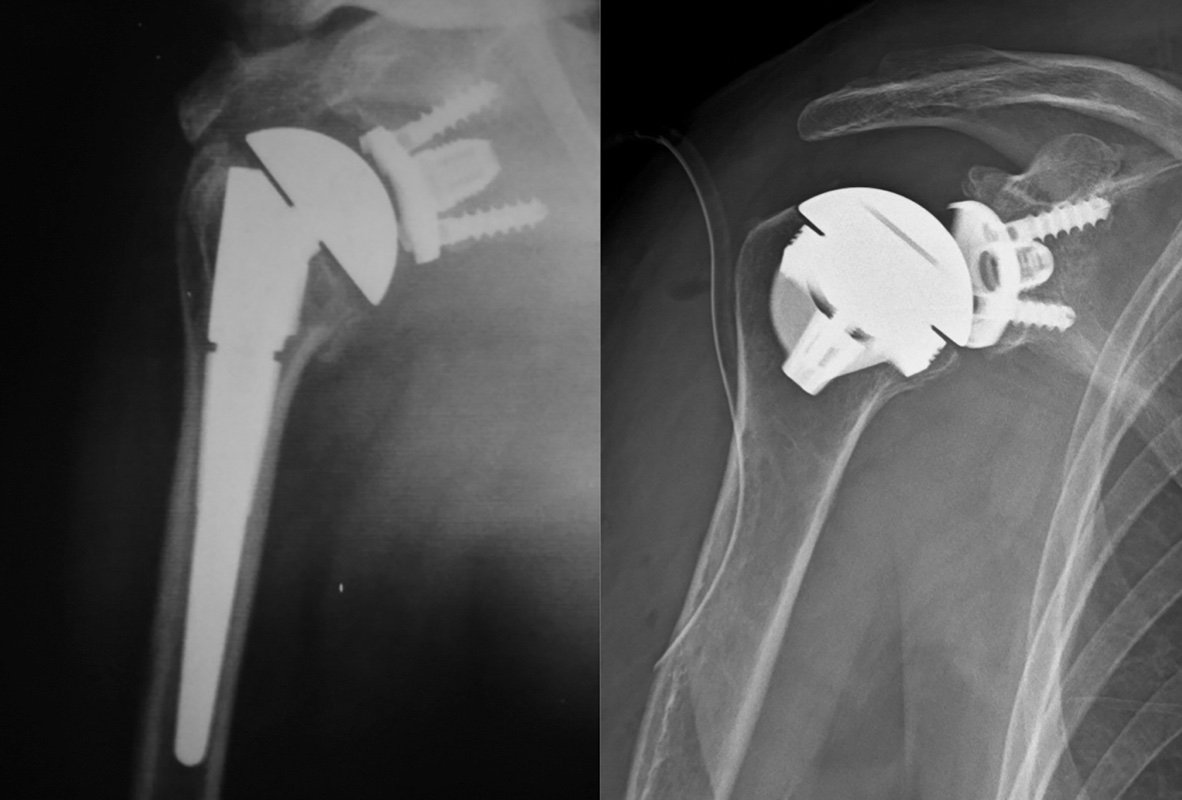
In commercio esistono protesi con stelo convenzionale, con stelo corto o senza stelo (Fig. 1).
L’esigenza di introdurre protesi con stelo corto, o addirittura assente, nasce dal desiderio di preservare osso meta-diafisario che inevitabilmente verrebbe a mancare immediatamente, durante la preparazione metafisaria e del canale midollare, o tardivamente per riassorbimenti legati allo stress shielding. Ovviamente una protesi a stelo corto o senza stelo è indicata in soggetti giovani dove si presuppone ci sia una buona qualità dell’osso metafisario e dove è possibile che in un futuro possa essere necessario un intervento di revisione protesica che, teoreticamente, così dovrebbe essere più semplice7.
La protesi anatomica può nel tempo fallire per una mobilizzazione asettica dello stelo protesico, ma soprattutto per la sopraggiunta rottura della cuffia dei rotatori. Quest’ultima può avvenire per la degenerazione tessutale che può essere legata all’età o alla concomitante presenza di patologie o stili di vita che possono alterare il microcircolo periferico (diabete ipertensione non controllata, ipercolesterolemia, sindrome metabolica, obesità, abitudine al fumo di sigaretta). Quando ciò si verifica, la testa protesica tende a migrare prossimalmente poiché non è più centrata nella glena per l’assenza della cuffia. In questi casi, e soprattutto nelle glene in polietilene cementate, si verifica la mobilizzazione glenoidea per il cosiddetto fenomeno del “cavallo a dondolo” ossia uno scollamento per una sollecitazione eccentrica della testa omerale protesica sul polietilene glenoideo.
Le protesi anatomiche di ultima generazione sono tutte convertibili, in corso di revisione, in protesi inverse. Ciò significa che lo stelo protesico può essere lasciato in situ e su di esso montare la coppa omerale e il “liner” della protesi inversa. Nel caso che al primo impianto fosse stata impiantata una glena con metal back e la revisione fosse dovuta alla migrazione prossimale della testa omerale senza mobilizzazione del metal back, quest’ultimo può essere lasciato in situ, limitandosi a sostituire il polietilene a incastro con una glenosfera adattabile.
PROTESI INVERSA
Poiché più facile da impiantare, rispetto alla protesi anatomica, e per i migliori risultati funzionali ottenibili nell’immediato post-operatorio, la protesi inversa rappresenta il 75% dell’impiantato nel mercato occidentale. L’impianto delle inverse era inizialmente indicato per la sola artropatia da cuffia; oggi le indicazioni si sono estese alle: rotture massive irreparabili cuffia con o senza pseudoparalisi; artropatie GO con cuffia sana; fratture complesse della testa omerale; sequele di fratture; osteonecrosi; lussazioni croniche irriducibili con deformità della testa omerale; neoplasie della testa omerale; artropatie infiammatorie e in fallimenti di endo/artroprotesi in giovani pazienti. Ovviamente è controindicata nei pazienti con lesione del nervo ascellare; deficit di diversa origine del muscolo deltoide; infezioni; immaturità scheletrica; malattie neuromuscolari che possano aumentare il rischio di instabilità protesica.
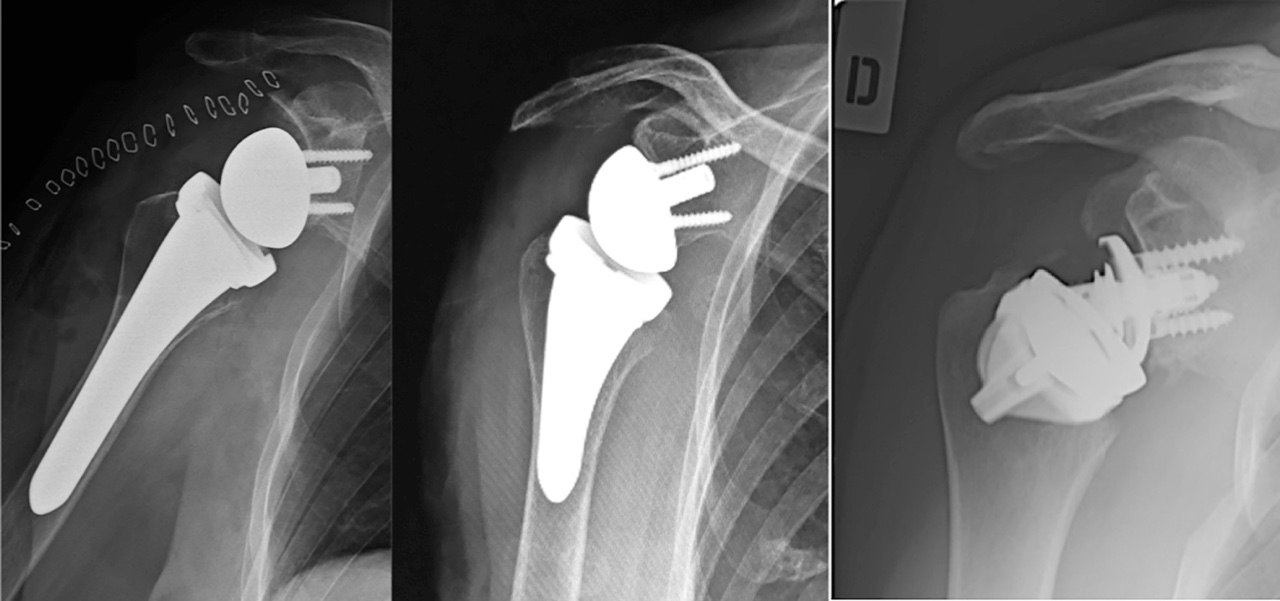
Dall’idea di Grammont (1985) la protesi inversa non ha subito grosse rivoluzioni per circa un ventennio. Una larga emisfera glenoidea e una componente omerale inclinata a 155° rispetto alla diafisi causano, rispettivamente, una medializzazione e un abbassamento del centro di rotazione. I principali problemi legati a questo impianto sono stati: lo scapular notching (contatto, e successiva usura ossea, tra il margine mediale della coppa omerale e collo scapolare) l’impingement, l’instabilità e l’usura del polietilene. La nuova generazione di protesi ha un angolo cervico diafisario di 135°-145° che ha ridotto la possibilità di impatto tra coppa omerale e collo scapolare8,9 (Fig. 2).
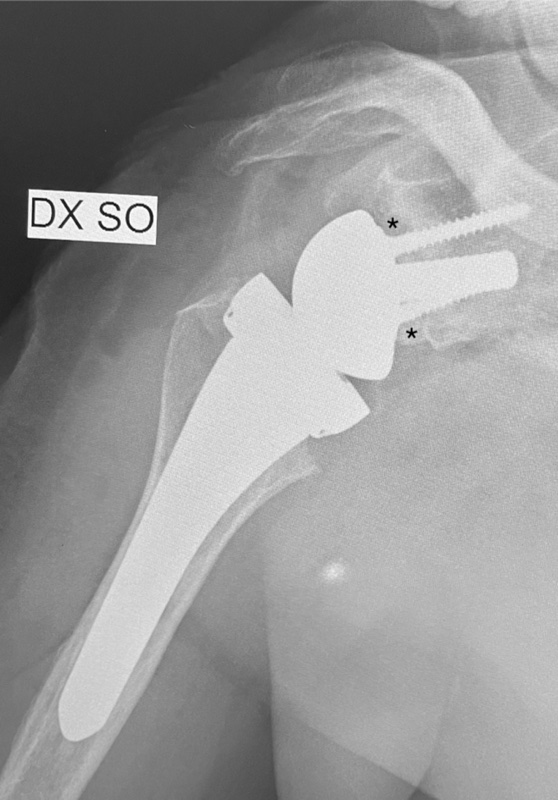
Lo stesso risultato può essere raggiungibile lateralizzando la glenosfera. Ciò può essere ottenuto o interponendo tra superficie articolare e metal back un tassello osseo prelevato o dalla testa omerale asportata o dalla cresta iliaca (BIO reverse)10 (Fig. 3), oppure creando un ulteriore spessore metallico.
Sorprendentemente, il tentativo di eliminare il fenomeno dello scapular notching ha portato a un inatteso incremento della mobilità post-operatoria. Un ulteriore incremento della mobilità può anche essere ottenuto impiantando glenosfere più grandi; tuttavia l’aumento delle dimensioni della glenosfera riduce lo spazio operatorio e rende particolarmente indaginosi alcuni passaggi tecnici.
Come per le protesi anatomiche, sono attualmente disponibili protesi con stelo standard, con stelo corto o senza stelo. Indubbiamente, la stemless ha una serie di vantaggi rispetto alla protesi a stelo classico: preservazione dell’osso metafisario e delle corticali diafisarie; assenza di complicanze legate alla presenza dello stelo (fratture periprotesiche); tempi operatori più corti; una teorica più facile revisione; possibilità di convertire in una protesi a stelo lungo o in una endoprotesi con testa omerale di grandi dimensioni e che abbia la possibilità di entrare in contatto con il margine antero inferiore dell’acromion (protesi CTA). A non renderle particolarmente popolari contribuisce il fatto che l’artropatia da cuffia, nel paziente giovane, è un evento raro.
CAPITOLO 39Bibliografia.
- Gumina S, Candela V. Rotator Cuff Arthropathy. What Is It? In: Gumina S. (eds) Rotator Cuff Tear. Cham: Springer 2017. doi: 10.1007/978-3-319-33355-7_46.
- Wirth MA, Rockwood CA Jr. Complications of total shoulder-replacement arthroplasty. J Bone Joint Surg Am. 1996 Apr;78(4):603-16. doi: 10.2106/00004623-199604000-00018..
- Gerber C, Pennington SD, Nyffeler RW. Reverse Total Shoulder Arthroplasty. J Am Acad Orthop Surg. 2009 May;17(5):284-95. doi: 10.5435/00124635-200905000-00003.
- Gumina, S., Candela, V. Clinical Evaluation. In: Gumina, S. (eds) Rotator Cuff Tear. Cham: Springer 2017. doi: 10.1007/978-3-319-33355-7_21.
- Rockwood CA Jr. The reverse total shoulder prosthesis. The new kid on the block. J Bone Joint Surg Am. 2007 Feb;89(2):233-5. doi: 10.2106/JBJS.F.01394.
- Nyffeler RW, Werner CW, Gerber C. Biomechanical relevance of glenoid component positioning in the reverse Delta III total shoulder prosthesis. J Shoulder Elbow Surg. 2005 Sep-Oct;14(5):524-8. doi: 10.1016/j.jse.2004.09.010.
- Castagna A, Delcogliano M, de Caro F, et al. Conversion of shoulder arthroplasty to reverse implants: clinical and radiological results using a modular system. Int Orthop. 2013 Jul;37(7):1297-305. doi: 10.1007/s00264-013-1907-4.
- Bohsali KI, Wirth MA, Rockwood CA Jr. Current Concepts Review: Complications of Total Shoulder Arthroplasty. J Bone Joint Surg Am. 2006 Oct;88(10):2279-92. doi: 10.2106/JBJS.F.00125.
- Sirveaux F, Favard L, Oudet D, et al. Grammont inverted total shoulder arthroplasty in the treatment of gleno-humeral osteoarthritis with massive rupture of the cuff: results of a multicentre study of 80 shoulders. J Bone Joint Surg Br. 2004 Apr;86(3):388-95. doi: 10.1302/0301-620x.86b3.14024.
- Gumina, S., Candela, V. (2017). New Concepts on the Glenoid Fixation in Reverse Shoulder Prosthesis. In: Gumina, S. (eds) Rotator Cuff Tear. Cham: Springer. https://doi.org/10.1007/978-3-319-33355-7_48.