Tendinopatia della cuffia dei rotatori
1Laboratorio di Biomeccanica Applicata, Dipartimento di Scienze Biomediche per la Salute, Università degli Studi di Milano, Milano, Italia; 2UOC 1a Clinica Ortopedica, ASST Centro Specialistico Ortopedico Traumatologico Gaetano Pini-CTO, Milano, Italia; 3REsearch Center for Adult and Pediatric Rheumatic Diseases (RECAP-RD), Dipartimento di Scienze Biomediche per la Salute, Università degli Studi di Milano, Milano, Italia
EPIDEMIOLOGIA
La tendinopatia della cuffia dei rotatori è la principale causa di dolore e disabilità alla spalla negli adulti, con una prevalenza crescente con l’età1. Studi radiologici mostrano che le lesioni parziali e a tutto spessore della cuffia dei rotatori aumentano significativamente dopo i 50 anni.
Lesioni asintomatiche sono presenti in meno del 15% degli individui nella quinta decade, nel 50% dei pazienti nella settima decade e nell’80% dei pazienti oltre gli 80 anni. La progressione delle lesioni e l’insorgenza di dolore sono comuni: il 61% dei pazienti con lesioni a tutto spessore e il 44% dei pazienti con lesioni parziali vanno incontro ad un peggioramento entro 3 anni. Inoltre, tra il 23% e il 51% dei pazienti con lesioni inizialmente asintomatiche sviluppano sintomi entro 1,5-3 anni2.
EZIOPATOGENESI
Le lesioni della CDR rappresentano un disturbo eterogeneo con un’eziologia multifattoriale. Possono essere causate da 3 diversi meccanismi patogenetici: estrinseco, intrinseco e traumatico.
Il meccanismo estrinseco, basato sulla teoria dell’impingement subacromiale di Neer, considera alla base della lesione il contatto ripetuto dei tendini della CDR (in particolare del sovraspinato) contro la parte anteriore dell’acromion e il legamento coraco-omerale. La riduzione dello spazio subacromiale può derivare da un impingement primario (ad esempio la presenza di un acromion ad uncino o di tipo III secondo la classificazione di Bigliani) o secondario (ad esempio una sublussazione superiore della testa omerale causata da cifosi dorsale e ipotonia muscolare).
Nel meccanismo intrinseco, le lesioni della CDR risultano come parte di un processo degenerativo legato all’invecchiamento e all’alterazione della micro-vascolarizzazione dei tendini.
Infine, le lesioni della CDR possono verificarsi a causa di un meccanismo traumatico che comprende traumi acuti ad alta energia (es. cadute a braccio teso) e microtraumi cronici (es. movimenti ripetitivi overhead durante attività sportive e lavori manuali). Le lesioni traumatiche acute sono più comuni nei soggetti giovani e spesso sono legate ad attività sportive e incidenti stradali3.
I principali fattori di rischio per le lesioni della CDR sono l’età, la genetica, le varianti anatomiche acromiali, il fumo e l’ipercolesterolemia. L’età è il fattore di rischio più significativo. Varianti anatomiche, come un acromion ad uncino o sporgente lateralmente, aumentano il carico sul tendine e di conseguenza il rischio di lesioni. Il fumo, riducendo la micro-vascolarizzazione del tessuto tendineo, aumenta non solo il rischio di rottura della CDR ma riduce anche le capacità di guarigione dei tendini e i risultati clinici dopo intervento chirurgico di riparazione. Infine, l’ipercolesterolemia compromette le proprietà biomeccaniche del tendine, aumentando il rischio di rottura.
CLASSIFICAZIONE
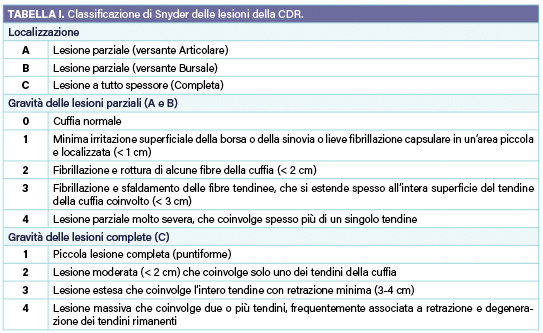
Negli anni sono stati proposti numerosi sistemi classificativi per descrivere le lesioni della CDR. Il sistema di classificazione più completo e utilizzato per le lesioni della CDR è la classificazione artroscopica di Snyder, che include una valutazione delle dimensioni, della localizzazione e della qualità dei tendini (Tab. I).
Altre due classificazioni che rappresentano importanti strumenti prognostici sono quelle di Thomazeau e Goutallier che valutano la qualità dei muscoli della CDR mediante, rispettivamente, risonanza magnetica nucleare (RMN) e tomografia assiale computerizzata (TAC).
La classificazione di Thomazeau definisce in 3 stadi l’atrofia del sovraspinato basandosi sulla porzione occupata dal muscolo nella fossa del sovraspinato nelle immagini sagittali T1 pesate in RMN (stadio 1: trofismo normale o lievemente ridotto; stadio 2: atrofia moderata; stadio 3: atrofia severa).
Goutallier, invece, classifica la degenerazione adiposa dei muscoli della CDR in 5 stadi in tagli assiali di TAC (stadio 0: muscolo normale; stadio 1: alcune strie adipose; stadio 2: < 50% di infiltrazione adiposa muscolare; stadio 3: 50% di infiltrazione adiposa muscolare; stadio 4: > 50% di infiltrazione adiposa muscolare). Più recentemente la classificazione di Goutallier è stata adattata per un utilizzo con la RMN.
PRESENTAZIONE CLINICA
I pazienti con una lesione della CDR spesso riferiscono dolore durante i movimenti della spalla e a riposo, specialmente di notte, oltre a debolezza muscolare e limitazione funzionale. L’ispezione del paziente, osservato posteriormente, può rivelare atrofia muscolare, soprattutto dell’infraspinato, e alterazioni della posizione e del movimento della scapola. È fondamentale valutare il range di movimento (ROM) attivo e passivo della spalla. Il dolore durante l’abduzione attiva tra 60° e 120° è un reperto comune (painful arc). Nelle lesioni massive della CDR può essere presente una spalla pseudoparalitica, definita come l’incapacità di elevare attivamente il braccio oltre i 45°. Un ROM passivo limitato è associato, invece, ad altre patologie della spalla, come artrosi gleno-omerale o capsulite adesiva.
Infine, devono essere eseguiti i test clinici specifici per valutare i singoli tendini della CDR (si veda il capitolo dedicato).
IMAGING
La diagnosi radiologica della tendinopatia della CDR si basa sull’utilizzo di radiografie convenzionali, ecografia e risonanza magnetica.
La radiografia, che deve comprendere due proiezioni (antero-posteriore e laterale “Y della scapola”), oltre a escludere altre patologie della spalla (come tendinopatia calcifica, artrosi gleno-omerale), può mostrare segni indiretti (ad esempio una migrazione superiore della testa omerale per rottura massiva della CDR) e fattori di rischio di lesioni della cuffia. Il parametro radiologico maggiormente predittivo per una lesione della cuffia è un Critical Shoulder Angle (CSA) > 35°. Il CSA è definito come l’angolo compreso tra l’asse della glenoide e la linea passante per il margine inferiore della glenoide e per il margine laterale dell’acromion.
L’ecografia è un esame diagnostico economico e non invasivo e consente una visualizzazione dinamica dei tendini della CDR durante i movimenti della spalla. L’ecografia ha una sensibilità del 92% e una specificità del 93% nel riconoscimento di lesioni a tutto spessore della CDR4. Tuttavia, è un esame operatore-dipendente e richiede una lunga curva di apprendimento, presentando così importanti limitazioni, in particolare nei pazienti con lesioni parziali di cuffia.
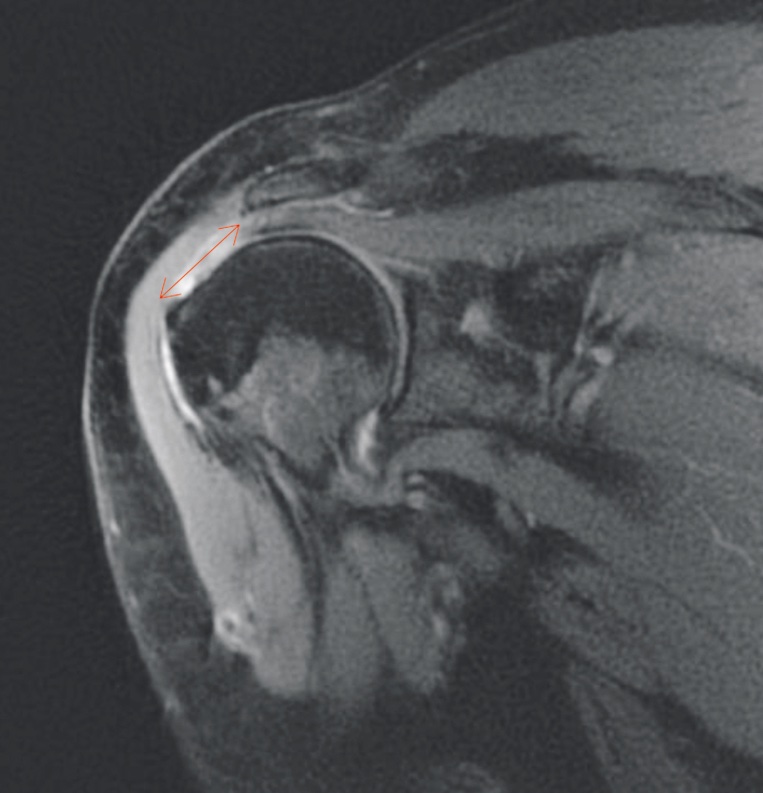
La risonanza magnetica è una tecnica più costosa, non invasiva, che consente di ottenere immagini ad alta risoluzione su più piani, sebbene statiche (Fig. 1).
La RMN mostra risultati simili a quelli dell’ecografia nel riconoscimento delle lesioni di cuffia a tutto spessore (94% di sensibilità e 93% di specificità), ma nei pazienti con lesioni parziali la sensibilità della risonanza magnetica è molto più alta di quella dell’ecografia (74% e 52%, rispettivamente) 4. Inoltre, la RMN è in grado di rilevare l’infiltrazione adiposa e l’atrofia dei muscoli della CDR. L’utilizzo del mezzo di contrasto (artro-RMN) non sembra migliorare l’accuratezza diagnostica della RMN ed è associata a maggiore invasività e discomfort per il paziente.
La tomografia computerizzata e l’artro-TAC sono attualmente poco utilizzate nella pratica clinica per diagnosticare le lesioni della CDR in quanto espongono il paziente a radiazioni ionizzanti senza apportare sostanziali benefici rispetto alla RMN.
TRATTAMENTO
Il trattamento delle rotture della CDR dovrebbe mirare a eliminare il dolore, migliorare il ROM e ripristinare la forza. Storicamente, nel trattamento delle lesioni della CDR veniva sempre consigliato un primo approccio conservativo, che comprende fisiochinesiterapia, FANS e infiltrazioni subacromiali. Tuttavia, studi recenti hanno definito meglio la storia naturale delle patologie della CDR, evidenziando il rischio di allargamento della lesione, la progressione della degenerazione adiposa muscolare e il declino funzionale nel tempo. Pertanto, sebbene un trattamento conservativo iniziale sia ancora un’opzione valida nella maggior parte dei pazienti, in alcuni casi un intervento chirurgico ritardato può presentare dei rischi5.
La fisioterapia include esercizi di mobilizzazione, stretching e rinforzo muscolare al fine di ripristinare l’articolarità e di prevenire le aderenze cicatriziali e la migrazione superiore della testa omerale. I FANS, sebbene efficaci nel breve termine, hanno effetti collaterali significativi che ne limitano l’utilizzo. Le infiltrazioni subacromiali, soprattutto di corticosteroidi, sono efficaci nel ridurre il dolore a breve termine, ma possono influire negativamente sulla guarigione dei tendini e aumentare il rischio di infezioni post-chirurgiche6. In alternativa, recentemente, le infiltrazioni di acido ialuronico (HA), di plasma ricco di piastrine (PRP) e di collagene hanno mostrato risultati promettenti nel medio-lungo termine con pochi o nulli effetti collaterali.
Nei pazienti in cui la terapia conservativa fallisce o con un rischio medio-alto di progressione della lesione, si raccomanda un trattamento chirurgico. Le opzioni chirurgiche dipendono dallo spessore e dalle dimensioni della lesione, dal numero di tendini coinvolti, dalla atrofia e dalla degenerazione adiposa muscolare, dall’età e dall’attività del paziente, dalle comorbidità e dalle preferenze del chirurgo.
Per le lesioni massive della CDR, le strategie chirurgiche includono debridement e decompressione subacromiale, riparazioni parziali, transfer tendinei, superior capsular reconstruction (con patch sintetico, autoinnesto o allotrapianto), riparazioni con utilizzo di augment, impianto di balloon subacromiale e protesi totale inversa della spalla.
Nelle lesioni parziali di basso grado, la decompressione subacromiale con semplice debridement della lesione può essere una strategia di trattamento sufficiente.
Nelle lesioni parziali sintomatiche di alto grado e nelle lesioni complete di piccola o media entità, la riparazione chirurgica del tendine è il trattamento più utilizzato, e può essere effettuata con tecnica open, mini-open o artroscopica. Quest’ultima è attualmente considerata il gold standard per il trattamento chirurgico delle lesioni della CDR.
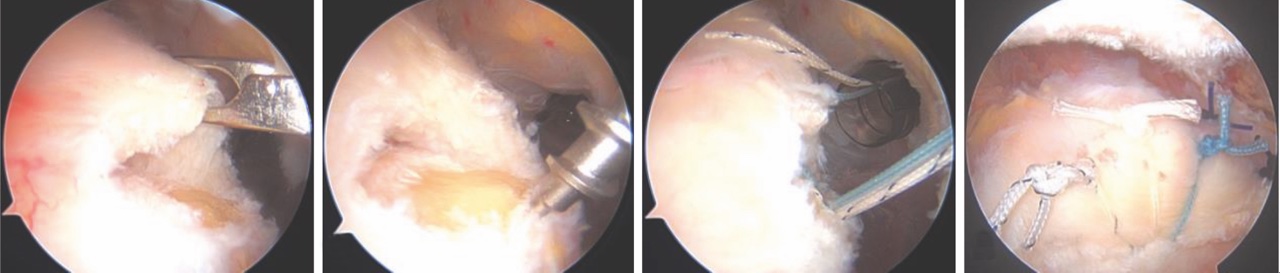
Nella tecnica artroscopica, sono disponibili diverse configurazioni di riparazione con utilizzo di ancore: Single-Row (SR – singola fila di ancore laterale) (Fig. 2), Double-Row (DR – doppia fila di ancore, una mediale e una laterale) e Suture Bridge (SB – doppia fila di ancore con suture incrociate che mimano una riparazione transossea).
Sebbene le riparazioni con doppia fila di ancore (DR e SB) abbiano dimostrato dei risultati biomeccanici migliori, con carichi di rottura più elevati e un miglior ripristino del footprint anatomico della CDR, non è ancora dimostrata una differenza significativa tra queste tecniche in termini di risultati clinici7. Inoltre, le tecniche DR, e in particolare la SB, hanno lo svantaggio di un costo maggiore.
La riparazione artroscopica della CDR ha mostrato, sia a breve che a lungo termine, buoni risultati clinici in termini di riduzione del dolore, recupero funzionale della spalla e ritorno alle attività quotidiane pre-trauma. Nonostante la soddisfazione dei pazienti raggiunga il 95% a 10 anni di follow-up, i tassi di ri-rottura tendinea post-operatoria rimangono alti (46%)8.
L’elevato numero di ri-lesioni dopo riparazione della CDR ha portato la ricerca scientifica a cercare di sviluppare approcci biologici innovativi per migliorare la guarigione del tendine. Tra questi, il più studiato è il PRP che, sebbene abbia un impatto favorevole sulla guarigione tendinea e sul tasso di ri-lesione delle lesioni di cuffia di piccole-medie dimensioni, non sembra migliorare i risultati clinici a lungo termine e, al costo attuale, non risulta vantaggioso nelle valutazioni di costo-efficacia9. Altri ortobiologici, tra cui vari fattori di crescita e le cellule staminali derivate da midollo osseo (BMSCs), tessuto adiposo (ADSCs), e tendine (TDSCs), stanno mostrando risultati incoraggianti in studi pre-clinici. Infine, particolarmente promettente sembra essere l’uso dei concentrati di midollo osseo autologo o di tessuto adiposo autologo che, rispetto ai fattori di crescita e alle cellule staminali, risultano essere molti più facili da utilizzare nella pratica clinica10.
CAPITOLO 35Bibliografia.
- Fehringer EV, Sun J, VanOeveren LS, et al. Full-thickness rotator cuff tear prevalence and correlation with function and co-morbidities in patients sixty-five years and older. J Shoulder Elbow Surg. 2008;17(6):881-885. doi: 10.1016/j.jse.2008.05.039.
- Lawrence RL, Moutzouros V, Bey MJ. Asymptomatic rotator cuff tears. JBJS Rev. 2019;7(6):e9. doi: 10.2106/JBJS.RVW.18.00149.
- Mall NA, Lee AS, Chahal J, et al. An evidenced-based examination of the epidemiology and outcomes of traumatic rotator cuff tears. Arthroscopy. 2013;29(2):366-376. doi: 10.1016/j.arthro.2012.06.024.
- Lenza M, Buchbinder R, Takwoingi Y, et al. Magnetic resonance imaging, magnetic resonance arthrography and ultrasonography for assessing rotator cuff tears in people with shoulder pain for whom surgery is being considered. Cochrane Database Syst Rev. 2013 Sep 24;2013(9):CD009020. doi: 10.1002/14651858.CD009020.pub2.
- Keener JD, Patterson BM, Orvets N, et al. Degenerative rotator cuff tears: refining surgical indications based on natural history data. J Am Acad Orthop Surg. 2019;27(5):156-165. doi: 10.5435/JAAOS-D-17-00480.
- Puzzitiello RN, Patel BH, Nwachukwu BU, et al. Adverse impact of corticosteroid injection on rotator cuff tendon health and repair: a systematic review. Arthroscopy. 2020;36(5):1468-1475. doi: 10.1016/j.arthro.2019.12.006.
- Rossi LA, Rodeo SA, Chahla J, et al. Current Concepts in Rotator Cuff Repair Techniques: Biomechanical, Functional, and Structural Outcomes. Orthop J Sport Med [Internet]. 2019 Sep 1;7(9):232596711986867.
- Randelli PS, Menon A, Nocerino E, et al. Long-term Results of Arthroscopic Rotator Cuff Repair: Initial Tear Size Matters: A Prospective Study on Clinical and Radiological Results at a Minimum Follow-up of 10 Years. Am J Sports Med. 2019;47(11):2659-2669. doi: 10.1177/0363546519865529.
- Feltri P, Gonalba GC, Boffa A, et al. Platelet-rich plasma does not improve clinical results in patients with rotator cuff disorders but reduces the retear rate. A systematic review and meta-analysis. Knee Surg Sports Traumatol Arthrosc. 2023;31(5):1940-1952. doi: 10.1007/s00167-022-07223-9.
- Randelli PS, Cucchi D, Fossati C, et al. Arthroscopic Rotator Cuff Repair Augmentation With Autologous Microfragmented Lipoaspirate Tissue Is Safe and Effectively Improves Short-term Clinical and Functional Results: A Prospective Randomized Controlled Trial With 24-Month Follow-up. Am J Sports Med. 2022;50(5):1344-1357. doi: 10.1177/03635465221083324.