Tecniche ricostruttive in ortopedia oncologica
Reparto di Ortopedia e Traumatologia II, Università di Pisa
MICROCHIRURGIA
Consiste nel prelevare in blocco da un sito donatore un segmento osseo (o un muscolo) lasciando intatto il suo periostio e i vasi nutritizi e transferirlo in altra sede ripristinando la vascolarizzazione mediante microanastomosi sui vasi del sito ricevente
Un trapianto vascolarizzato ha in se tutte le 5 caratteristiche ideali richieste a una ricostruzione bioogica: è uno scaffold (osteoconduzione) , conserva i suoi intrinseci growth factors (osteoinduzione delle BMP) ,mantiene cellule-osteociti e osteoblasti- vitali con una rete vascolare efficiente (osteogenesi) e inoltre ha importanti proprietà biomeccaniche e fisiche di adattamento a stimoli esterni (carico, campi magnetici etc). Si calcola che circa l’80% degli osteociti sopravvivano dopo il trapianto contro il 5-20% di quanto avviene negli innesti autoplastici non vascolarizzati
La microchirurgia trova indicazione in tre situazioni particolari:
- ricostruzione intercalari o artrodesizzanti
- ricostruzioni articolari speciali:
- trapianto epifisario con la cartilagine di accrescimento nel bambino;
- artroplastica biologica nell’adulto.
- trapianto di unità motoria per ricostruzioni muscolari.
Nelle ricostruzioni intercalari o artrodesizzanti il segmento osseo più utilizzato è il perone prelevato assieme alla arteria peroniera. In effetti vi sono i seguenti vantaggi:
- il perone ha una lunghezza comparabile alla tibia e al femore (e quindi permette di affrontare lunghe resezioni delle ossa maggiori;
- può essere prelevato con la cute sovrastante (osteocutaneo) o muscolo (osteomuscolare) in caso di ricostruzioni combinate;
- le sequele funzionali nel sito donatore sono usualmente minime. Si consiglia intensa mobilizzazione dell’estensore proprio dell’alluce per evitarne la retrazione. In caso di prelievo dell’epifisi prossimale, il collaterale laterale e il bicipite vengono reinseriti sulla tibia. È opportuno conservare l’estremità distale del perone (sezionando sopra la sindesmosi) e stabilizzare la T.T. con vite e innesto intertibioperoneale;
- la consolidazione a livello di osteotomia è di solito abbastanza rapida (3-4 mesi);
- il mantenere una intatta vascolarizzazione endostale fa si che questi segmenti intercalari guariscano in maniera simile a quello che avviene in traumatologia nelle fratture segmentarie bifocali con una consolidazione possibile anche se rallentata soprattutto in un polo. Una cuffia di periostio attorno all’osteotomia favorisce la fusione. La consolidazione può essere conseguita con una osteosintesi di minima all’arto superiore (se il segmento è infisso nella metafisi); nell’arto inferiore è necessaria una osteosintesi stabile di supporto e a ponte;
- il trapianto sotto carico progressivo può andar incontro a una ipertrofia corticale con apposizione di osso periosteo. Tale crescita non supera mai le dimensioni originali del segmento sostituito;
- il processo di ipertrofia è tuttavia molto lento (anni) tenendo conto che la tibia è 3 volte e il femore 5 volte più spesso. Talora è un processo lento ma armonico; talora avviene invece mediante fratture ripetute che aumentano la morbidità (fratture da stress) o sono potenzialmente pericolose (in caso di scomposizione grave richiedono un intervento chirurgico).
Per accelerare il processo di ipertrofia vi sono tre tecniche:
- double barrel: viene utilizzato per difetti di < 10 cm. Dal perone prelevato, lasciandone intatto e continuo il periostio e il vaso nutritizio, viene asportato un cm centrale. I due segmenti vengono poi ripiegati a canna di fucile: si ottiene così un doppio perone con una unica anastomosi;
- perone vascolarizzato con membrana periostea: viene utilizzato per difetti lunghi> 10 cm. Il perone viene prelevato per tutta la lunghezza possibile in continuità con un lembo fasciale costituito dal periostio anterolaterale della tibia e dalla membrana interossea. Entro questo flap vengono inserite chip ossee e il flap richiuso su stesso (camera biologica). Si ottengono così due strutture lunghe ed appaiate
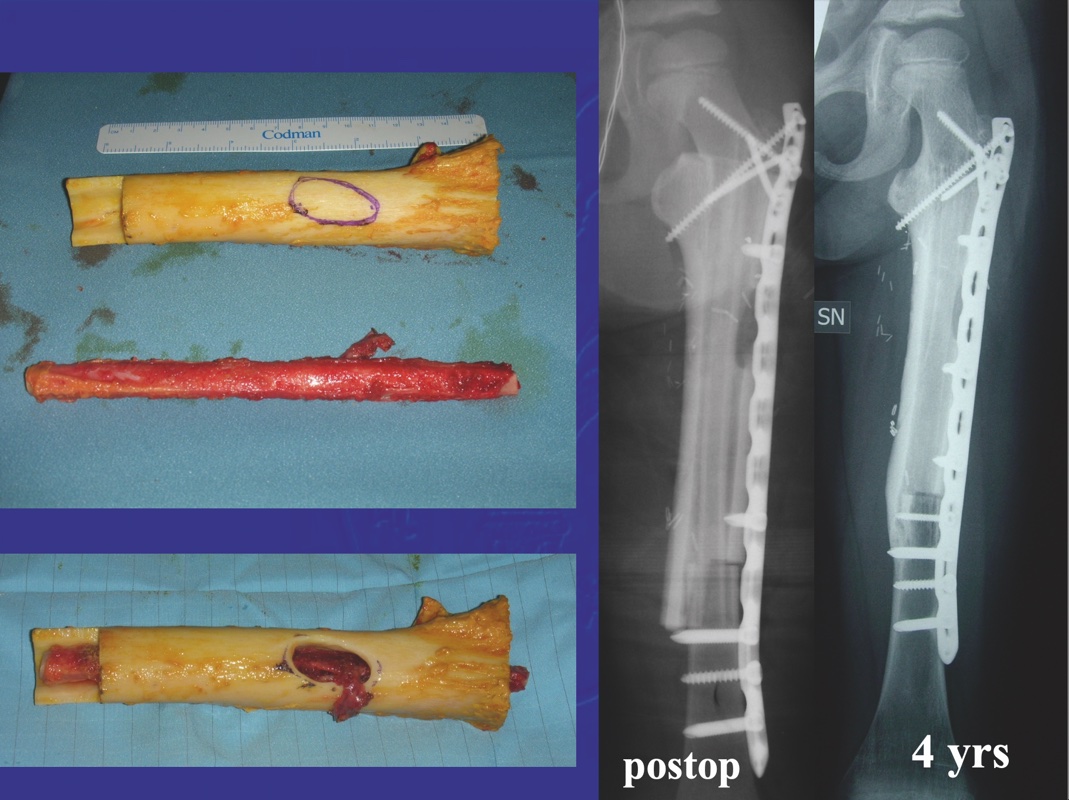
- associazione perone vascolarizzato e trapianto massivo (“Capanna Technique”, Fig. 1).
Si basa sulla sinergia delle due componenti che si compensano a vicenda nel tempo.
Il trapianto massivo è inerte, non vitale e anche se in seguito a fenomeni di creeping substitution può avere riassorbimenti tardivi e fratture, nell’immediato fornisce la necessaria forza e stabilità all’impianto. Il perone è debole e soggetto a fratture precoci, ma essendo un osso vivo, fornirà invece nel tempo riparazione ossea e ipertrofia progressiva.
Può essere eseguita osteosintesi di minima con viti (resezioni intraepifisarie) o con placche limitata alle zone osteotomiche (resezioni metafisarie): peraltro ogni volta sia possibile si raccomanda una osteosintesi a ponte.
Nelle ricostruzioni tibiali e femorali distali, il perone viene inserito all’interno del trapianto tramite una lunga finestra ossea (in questi casi l’asse anatomico e di carico coincidono, il peduncolo vascolare è vicino, l’osteosintesi di supporto è limitata e si evitano problemi di chiusura cutanea). Nelle ricostruzioni femorali prossimali il perone è di solito posto medialmente al trapianto (in questi casi, l’asse di carico è spostato medialmente, il peduncolo è mediale, è possibile una valida osteosintesi di supporto sulla corticale laterale e non vi sono problemi di chiusura cutanea.
Nel tempo si assiste a una ipertrofia del perone che coinvolge e determina anche una riabitazione ossea del trapianto massivo (favorita anche dalla finestra ossea che espone la superfice endostale ai fenomeni riparativi.).
La tecnica permette di diminuire le pseudoartrosi a livello delle osteotomie (frequenti nei trapianti massivi) e le fratture (frequenti nei peroni vascolarizzati). In una recente metanalisi fra le varie tecniche ricostruttive intercalari è risultata quella con la maggiore probabilità di successo.
Trova indicazione nelle ricostruzioni più difficili ove è minimo il bone stock residuo (resezioni iuxtaarticolari; resezioni intraepifisarie; salvataggio della cartilagine di accrescimento) o nelle resezioni lunghe diafisarie (> 14 cm) degli arti inferiori.
Ricostruzioni articolari speciali:
- trapianto epifisario con la cartilagine di accrescimento nel bambino.
- La tecnica si prefigge di ricostruire un’estremità articolare nel bambino utilizzando un perone vascolarizzato ma mantenendo la sua cartilagine di accrescimento intatta e vitale nell’intento di salvaguardare la crescita dell’arto.
- I primi tentativi che utilizzavano il perone con l’arteria peroniera furono fallimentari. La constatazione che la vascolarizzazione della cartilagine di accrescimento era supportata da un ramo ricorrente della arteria tibiale anteriore portò a una modifica del prelievo (peduncolo basato sulla tibiale anteriore) con importanti vantaggi sull’esito dell’intervento. Tale prelievo peraltro è particolarmente complesso in quanto il vaso da salvaguardare passa attraverso i rami dell’SPE.
- Alla zona di osteotomia il perone può essere apposto (face to face) all’osso ospite per aumentare la superficie e favorire la consolidazione. Il perone va protetto lungo tutto il suo decorso con una placca e rare viti monocorticali.
- Tale trapianto fu attuato in diversi piccoli pazienti sia all’omero prossimale che al radio distale. Si è osservato una crescita dell’osso trapiantato nel 70 /80% dei pazienti; la crescita è stata di circa 0.7-1cm all’anno. La motilità attiva della spalla e del polso furono ottime dopo semplice capsuloplastica a borsa di tabacco attorno all’epifisi. Si è osservato nel tempo un progressivo rimodellamento della epifisi del perone che ha preso la morfologia concava del radio distale (al polso) o l’inclinazione con comparsa di pseudotrochite (alla spalla).
- Tale tecnica, anche se talora eseguita, non è consigliabile all’arto inferiore (anche quando associata a trapianti massivi di sostegno) per esiti imprevedibili e frequenti complicanze meccaniche.
- Artroplastica biologica nell’adulto
Varie ricostruzioni sono state descritte utilizzando altri segmenti ossei vascolarizzati:
- cresta iliaca vascolarizzata pro-calcagno;
- 2° metarso pro 1 metacarpo;
- articolazione metatarso falangea pro-gomito;
- accoppiamento di banco (cresta iliaca vascolarizzata+ perone vascolarizzato) pro-omero distale.
Trapianto di unità motoria per ricostruzioni muscolari
Accanto ai lembi liberi cutanei o muscolari di copertura a tutti ben noti) un ruolo interessante hanno i trapianti di unità motoria:
- La tecnica consiste nel prelevare un muscolo con il suo peduncolo vascolare e il suo nervo motore e trapiantarlo a vicariare un muscolo asportato ripristinando non solo la vascolarizzazione (copertura biologica) ma anche l’innervazione (funzione contrattile).
- Gli interventi più frequenti sono il muscolo gran dorsale pro-quadricipite (sutura su nervo femorale) o pro-estensori piede (sutura su SPE) o pro tricipite surale (sutura su SPI) o pro estensori polso e dita (su radiale).
- Poiché sia il nervo del lembo e quello recipiente sono entrambi motori la reinnervazione è di solito efficiente.
- Poiché il nervo del gran dorsale è corto la reinnervazione è abbastanza rapida.
- Nell’applicare e fissare il muscolo trapiantato al letto recipiente occorre porre molta attenzione che la tensione del muscolo sia appropriata, paragonabile a quella del muscolo asportato (ovvero sia non deteso, sia non stirato) 1,2.
TRAPIANTI MASSIVI OMOPLASTICI
L’allotrapianto massivo presenta diversi vantaggi (la ricostituzione del bono stock osseo, l’ancoraggio biologico tendine-tendine) e sono utili nelle ricostruzioni intercalari. Ma hanno anche molti svantaggi (lento recupero funzionale, ritardato carico, degenerazione nel tempo della superfice articolare, alto tasso di pseudoartrosi e fratture).
I Trapianti massivi vengono prelevati e conservati sterilmente in supercongelatori a -80 gradi o in azoto liquido in Banche certificate. Tali Banche garantiscono inoltre l’idoneità del donatore, la presenza di esami sierologici e colturali accertanti la sterilità del trapianto e la non trasmissibilità di malattie, eseguono il monitoraggio e la registrazione continua della adeguata conservazione (che può protrarsi fino a 5 anni) , e infine registrano mediante misurazioni Rx o TC la consistenza /spessore dei trapianti stessi, la presenza di capsule o legamenti inseriti, la loro morfologia articolare. Tali misure sono essenziali per la ricerca del trapianto idoneo che deve riprodurre millimetricamente il segmento asportato (tale criterio è vincolante nei trapianti osteoarticolari ma molto meno nelle protesi composite). I trapianti massivi essendo privi o privati del midollo osseo non richiedono il rispetto della istocompatibilità: anche se vi può essere una risposta anticorpale essa è di solito subclinica. La crioconservazione diminuisce inoltre tale reazione.
Biologicamente i trapianti massivi presentano le seguenti caratteristiche e le seguenti problematiche.
Rischi Infettivi. Erano molto alti in passato con i trapianti freschi o conservati a -40°. L’avvento di banche qualificate con opportuna selezione dei donatori, valutazione della sterilità e adeguata conservazione dei trapianti, nonché una antibioticoterapia peri-operatoria aggressiva e prolungata e una particolare cura alla copertura cutanea (lembi liberi o peduncolati) hanno nettamente diminuito tale incidenza, portandola al livello osservato nelle megaprotesi (circa 10%). In questi interventi complessi il rischio infettivo sembra essere più legato agli ampi accessi chirurgici, alla exeresi muscolari, alle perdite ematiche, ai tempi operatori, allo stato delle difese immunitarie del paziente (chemio /radioterapia) che alla tipologia dell’impianto ricostruttivo.
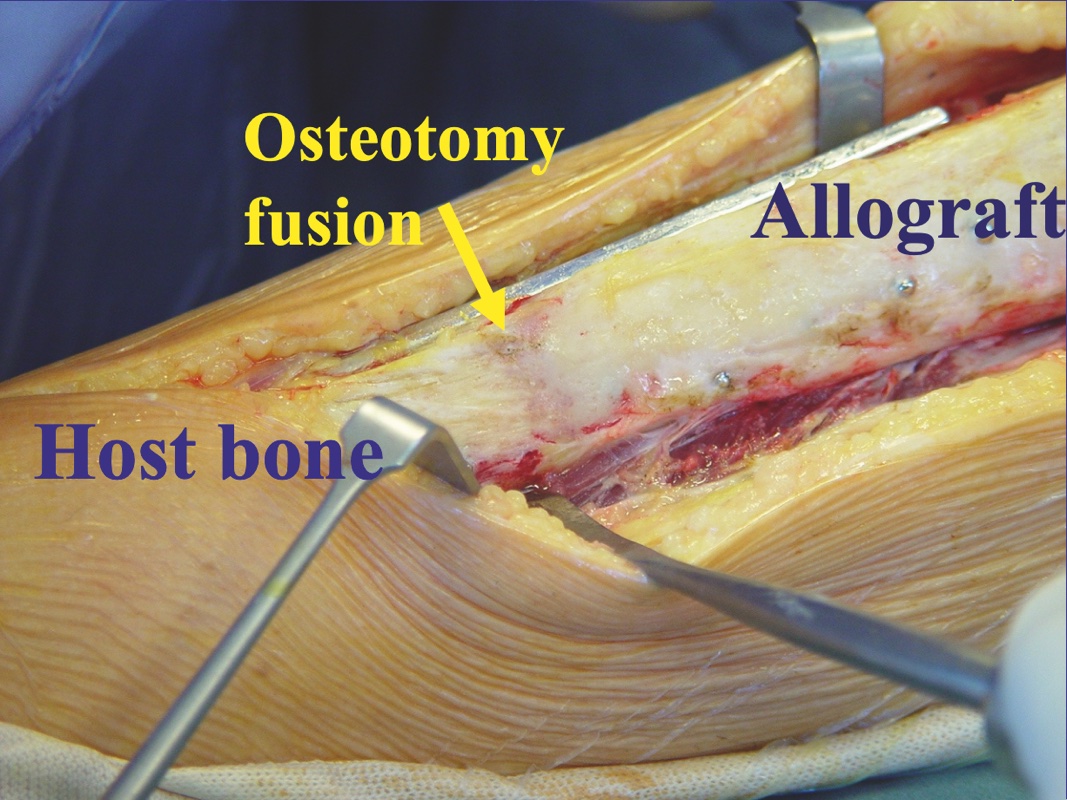
Consolidazione. È un processo lento (fino ad un anno). La fusione avviene mediante callo periostale ed endostale con interdigitazioni di osso vitale (ospite) nell’ osso non vitale (trapianto) per una profondità di circa 25 mm (Fig. 2).
La fusione è favorita da: 1) contatto perfetto e stesso calibro; 2) aumento della superfice di contatto (sezioni oblique o a Z, apposizione face to face) ;2) osteosintesi stabile e rigida;3) apposizione di innesti autoplastici (soprattutto se dilazionati) ;4) copertura con flap di periostio o materiale osteoinduttivo; 5) viene ritardata dalla chemioterapia e inibita dalla radioterapia. Il rischio di pseudoartrosi è valutabile intorno al 25-30%, più basso nei bambini (15%) maggiore nelle artrodesi (oltre 50%). La pseudoartrosi è rara quando sono giustapposte due superfici spongiose (0-9%) mentre è molto più frequente (fino 50%) nel contatto corticale -corticale. L’uso di osteosintesi dinamica (chiodi bloccati) aumenta il rischio di pseudoartrosi. La pseudoartrosi è una complicanza che richiede un reintervento ma che difficilmente porta al fallimento.
Riabitazione ossea. Un trapianto osseo massivo chiuso presenta una osteogenesi riparativa solo alla sua superfice esterna e in maniera molto limitata (1-2mm) mentre l’interno rimane non vitale con lacune osteocitarie e canali Haversiani vuoti e acellulari. Anche nei controlli a distanza di vari anni solo il 20% del trapianto dimostra una riabitazione (ad eccezione dei bambini molto piccoli in cui la riabitazione può essere completa). Il trapianto va incontro a un fenomeno di “creeping substitution” che determina nel tempo un calo del suo modulo di flessione, un aumento delle microfratture interne e un decremento della sua resistenza meccanica (-11.144 ogni anno). A distanza di 10 anni, la corticale perde il 50% della sua resistenza, ha un aumento pari a 6 volte di microfratture, e un aumento del 20% di porosità. Da qui la necessità di armare il trapianto per tutta la sua lunghezza con una valida osteosintesi di supporto. Questa erosione continua espone nel tempo il trapianto a fratture. Le fratture sono suddivise in 3 tipi. Tipo1: molto rara (< 1%) , precoce (di solito entro il primo anno) caratterizzata da uno sgretolamento improvviso del trapianto per una possibile reazione immunologica, e ne richiede la rimozione; Tipo2: più frequente ma più tardiva (2°-3° anno) ,localizzata nella parte intermedia e dovuta alla creeping substitution con riassorbimenti parziali, spesso legata anche a errori tecnici (inadeguata osteosintesi, esecuzione di fori di ancoraggio per reinserzioni capsulo-legamentose, trapianto osteoporotico, o irradiato) , richiede quasi sempre un reintervento, talora conservativo (nuova osteosintesi e grafting) più spesso (80%) una sostituzione del trapianto; Tipo3: tardiva (oltre 3 anni) consiste in fratture articolari o subarticolari. favorite dalla rivascolarizzazione dei tessuti molli periarticolari con erosioni del bordo articolare, incongruenze morfologiche, deviazioni assiali, instabilità articolare e richiede la protesizzazione (conversione in protesi composita). Per diminuire il rischio di fratture vi sono tre possibilità diverse:
- riempire di cemento il canale midollare del trapianto. Oltre a rinforzare il trapianto permette una migliore presa delle viti di una eventuale placca esterna di sostegno e se il cemento è antibiotato può essere utile nel controllo infettivo. Peraltro, non riesce a proteggere la parte subarticolare di un trapianto osteoarticolare;
- nelle ricostruzioni articolari utilizzare una protesi composita;
- nelle ricostruzioni intercalari potenziare invece la biologia e la riabitazione ossea esponendo anche la parte endostale del trapianto (ricostruzione con stecche corticali multiple a fascio; associazione trapianto massivo e perone vascolare).
Riabitazione capsulo-legamentose. Le strutture capsulo-legamentose del trapianto si integrano perfettamente a quelle dell’ospite con una frequente colonizzazione cellulare da parte del ricevente. Questo è il grande vantaggio dei trapianti ostearticolari e il motivo del ricupero di una motilità attiva ottimale, non ottenibile con altre ricostruzioni protesiche. È importante selezionare trapianti osteoarticolari che abbiano tali inserzioni tutte conservate e “ritagliabili “sul campo operatorio secondo necessità. Va privilegiata la sutura termino terminale o a cappotto di tali elementi eseguite con suture non riassorbibili L’integrazione capsulo-legamentosa è lenta e va protetta a lungo (il doppio di quello che si usa per le ricostruzioni tendinee autoplastiche). I risultati funzionali, ottimi inizialmente, possono degradare nel tempo quando il tessuto riparativo raggiunge la base di impianto e determina erosioni ossee. La reinserzione della capsula e dei legamenti tramite tunnel ossei nel trapianto va sempre evitata perché espone a fratture e sarebbe una sutura in tensione prona al distacco.
Evoluzione cartilagine articolare omoplastica. Anche se la cartilagine viene trattata e ricoperta con sostanze crioprotettrici durante la conservazione, dopo l’impianto si assiste a un deterioramento progressivo della stessa con comparsa di laminazioni, vacuoli, erosioni, sostituzione con tessuto fibro-ialino, e talora ulcerazioni. Tale degenerazione spesso non si accompagna a un peggioramento clinico (dolore) essendo il trapianto non innervato. Questo peraltro può innestare una evoluzione simile alle Charcot Joint. Tale degenerazione è tempo dipendente (44% < 2 anni; 83% oltre 2 anni ed è molto più evidente negli arti inferiori ed è favorita da una incongruenza dimensionale o una instabilità articolare. In più la cartilagine (priva di vasi e come tale non immunogena) in seguito ai fenomeni degenerativi e alla neo angiogenesi del tessuto reattivo può diventare immunogena, con comparsa di un panno sinoviale erosivo periarticolare.
Indicazioni attuali dei trapianti massivi
Attualmente trovano indicazione:
- in maniera elettiva nelle resezioni intercalari e in quelle artrodesizzanti (da soli o rinforzati con cemento o eventualmente associati a perone vascolarizzato);
- in maniera selettiva nelle ricostruzioni articolari nelle seguenti situazioni:
- resezione emiarticolare del ginocchio (emicondili o emipiatti tibiali). Il trapianto opportunamente sagomato permette di ricostruire anatomicamente l’articolazione conservando l’altra estremità. L’ampia superfice di contatto permette una consolidazione sicura e una riabitazione importante; il reinserimento dei legamenti e della capsula, garantisce la stabilità articolare; la placca di sostegno mette al riparo da fratture. I risultati anche a distanza di decenni sono particolarmente buoni;
- sedi finora considerate non ideali per ricostruzioni protesiche (scapola, emi pelvi, radio distale, ulna prossimale, ossa tubulari mano e piede). In tali sedi recentemente vi è l’alternativa e la competizione delle protesi custom made 3D: i dati sono ancora troppo recenti e sporadici per trarre conclusioni comparative;
- sedi in cui si voglia massimizzare i risultati funzionali tramite un più esteso ed efficiente ancoraggio muscolo-tendineo. Queste sedi sono:
- il femore prossimale (reinserzione glutei e ileo-psoas);
- l’omero prossimale (reinserzione cuffia rotatori, gran dorsale e capo lungo bicipite);
- l’omero distale (reinserzione tricipite, epicondiloideei ed epitrocleari);
- la tibia prossimale (reinserzione tendine rotulreo, flessori mediali).
Ovviamente l’indicazione è nei pazienti in cui la neoplasia (o il danno) sia intraossea per cui è possibile una resezione rispettosa di tali strutture. Come si vede non è presente il femore distale, sede in cui non vi sono significanti inserzioni muscolo tendinee. Tuttavia, per ovviare le complicazioni dei trapianti osteoarticolari sopra descritte, in tali sedi attualmente vengono preferite le protesi composite;
- Protesi composite. La protesi composita (tipo A) è la più comune ed è data dalla combinazione di una protesi da revisione a stelo lungo con un trapianto massivo dotato delle sue inserzioni tendinee periarticolari. Il trapianto viene preparato su tavolino per alloggiare la parte metadiafisaria prossimale della protesi che viene fissata al trapianto stesso con cemento acrilico (essendo il trapianto un segmento inerte e non vitale sarebbe errato puntare su superfici porose per bone ingrowth). Lo stelo che protrude dalla zona osteotomica per almeno 13 cm viene inserito nel canale midollare dell’ospite e fissato o con cemento o mediante press fitt (seguendo le indicazioni che verranno riportate nelle megaprotesi) L’obbiettivo è quello di minimizzare con la protesi le complicazioni dei trapianti, mantenendo i pregi di quest’ultimi. Infatti:
- l’articolazione protesica garantisce la stabilità articolare ed evita i fenomeni di degenerazione articolare e le fratture articolari tipo 3;
- lo stelo protesico e il cemento rinforzano l’allograft evitando le fratture di tipo 2;
- la consolidazione a livello osteotomico non è strettamente necessaria: se avviene è migliorativa prolungando la superfice di contatto e di presa della protesi. Qualora esitasse in pseudoartrosi, la ricostruzione non fallisce per la presenza dello stelo nella diafisi distale del ricevente (l’impianto funziona come una megaprotesi a fissazione distale);
- nella zona ove è presente l’allograft, la doppia interface stelo- cemento e cemento- corticale interna del trapianto è inerte e avascolare (quindi stabile e difficilmente infiltrabile da debrids protesici o suscettibile di rimaneggiamenti e riassorbimenti ossei reattivi). La corticale esterna del trapianto è ricoperta invece da un sottile strato di osteogenesi (1-2 mm) che si continua con un neoperiostio e l’ancoraggio muscolo -tendineo (tendine su tendine). Questa interfaccia biologica (pregio dei trapianti osteoarticolari) è estremamente efficace e garantisce un eguale ottimo recupero funzionale. Nelle megaprotesi si tenta di ottenere un risultato simile usando rivestimenti o camicie di rivestimento porosi (tantalium,etc) ma con minor efficacia non avendo incorporati le inserzioni tendinee naturalmente presenti nei trapianti.
La protesi composita tipo B prevede una protesi tutta inserita nel trapianto mentre la zona osteotomica riproduce quella dei trapianti tradizionali affrontando semplicemente le due superfici, stabilizzate con placca. Sono raramente utilizzate (quando la resezione è molto lunga e non vi è spazio per uno stelo midollare e soprattutto nei bambini) 3,4.
MEGAPROTESI MODULARI
Le megaprotesi sono l’approccio ricostruttivo di più largo utilizzo nella chirurgia ortopedica ricostruttiva moderna e trovano impiego in pazienti soggetti a resezione ossea per tumori, traumi freschi o esiti di traumi maggiori con estesa perdita di bone stock, pseudoartosi ribelli, o revisione complesse di artroprotesi. Le prime megaprotesi custom made furono prodotte negli anni 1950-60, ed erano progettate a partire dalle immagini radiografiche del paziente, così da replicare accuratamente forma e dimensione dell’osso da sostituire. Da un punto di vista produttivo, venivano forgiate da un unico blocco metallico di acciaio o titanio. Sebbene questo approccio garantisse a tali impianti una resistenza considerevole ed una forma spesso corretta, la natura mono-blocco di queste protesi ne limitava in modo significativo l’adattabilità intraoperatoria, rendendo impossibili variazioni di lunghezza di resezione, scelta di steli diversi (per dimensione, lunghezza, spessore e tipologia di ancoraggio) ,e la correzione intraoperatoria delle rotazioni se sbagliate. Richiedevano inoltre tempi lunghi di esecuzione (la chemioterapia preoperatoria venne introdotta in tali anni proprio nell’intenzione di fermare la crescita tumorale in attesa della protesi).
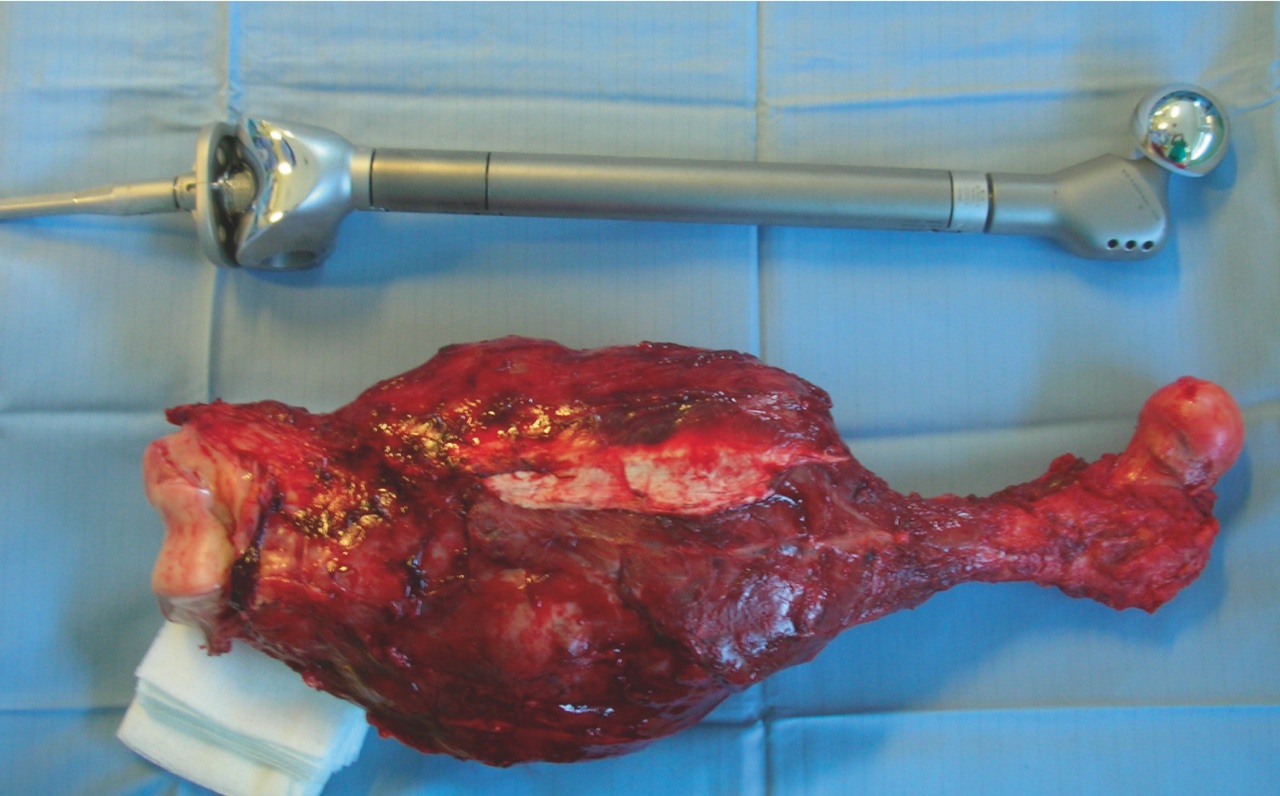
Questo limite venne superato, negli anni 1980-90, con l’introduzione delle moderne megaprotesi modulari costituite da più segmenti componibili di varie forme e dimensioni, disponibili sterili e assemblabili sul campo operatorio sulla base delle richieste anche estemporanee del chirurgo (Fig. 3).
La modularità è tale da poter consentire al chirurgo di cambiare il tipo di ricostruzione in corso d’opera, passando da una megaprotesi convenzionale articolata ad una protesi composita (con aggiunta di allograft) oppure ad un impianto artrodesizzante o – se necessario – intercalare.
La possibilità di disporre di una strumentazione unica, versatile per tutte le necessità e sempre disponibile ha annullato i tempi d’attesa per lo svolgimento di interventi chirurgici, come quelli oncologici, in cui il fattore tempo gioca un ruolo fondamentale.
Schematicamente, le megaprotesi possono essere suddivise in tre componenti fondamentali: (1) componente articolare, (2) prolunghe o segmenti intercalari e (3) steli
Componente articolare e peri-articolare
Ricostruisce la zona epifisaria e metafisaria. Usualmente tale componente viene fornita in varie misure sia di lunghezza che di grandezza.
Nel femore prossimale la articolarità è garantita da un tronco di cono che può raccordarsi tramite testine convenzionali (22,28,32) a scelta con ogni tipo di coppa acetabolare standard, o con endo protesi bipolari, o con coppe a triplice motilità. Queste due ultime soluzioni sono preferibili per aumentare la stabilità dell’impianto ed evitare lussazioni postoperatorie (frequenti-25%-in seguito al distacco dei muscoli pelvi trocanterici e all’asportazione della capsula articolare). La possibilità di avere componenti articolari con diverso offset permette di agire e migliorare la tensione muscolare. La presenza di una vite verticale di assemblaggio con le componenti di prolunga è anche essa utile per modificare in qualsiasi momento l’antiversione o retroversione articolare in caso siano errate (causa di insufficiente copertura o di eventuale impingement). Le parti articolari presentano fori per il reinserimento muscolare dei glutei e talora dell’ileo psoas. L’adesione dei muscoli alla protesi metallica è utopica. Di solito attorno alla protesi si forma un guanto fibroso (separato dal metallo da una sottile interlinea a contenuto liquido) cui si attaccano i muscoli e tramite cui essi esplicano la loro azione in maniera indiretta. Questa (oltre l’eventuale escissione muscolare oncologica) è la causa dell’insufficienza glutea (Trendelemburg) di questi pazienti Una migliore adesione si ottiene con superfici porose madreporiche o tridimensionali (fibrometal, tantalio etc) poste in superficie che peraltro non presentano metodi di inserzioni tendinee dirette (o loro equivalenti artificiali). Aumentare cospicuamente la superficie di contatto con strutture porose in protesi che hanno già di per sé grandi dimensioni può determinare un rilascio ionico cospicuo. L’uso di protesi composite garantisce una superfice biologica e il ripristino di una azione diretta dei muscoli sul segmento articolare con evidente recupero funzionale. Un sistema valido e veramente flessibile dovrebbe dunque disporre di componenti articolari metalliche a spessore ridotto (da inserire in trapianti osteo tendinei) sia a spessore convenzionale (megaimpianti).
In caso di mega protesi convenzionale si consiglia di ancorare “temporaneamente” i musco.li ai fori protesici ma anche di suturare direttamente e in continuità i glutei con il quadricipite e il tensore della fascia lata (tension band) in modica abduzione.
Nell’omero prossimale i concetti riproducono quelli dell’anca: 1) La componente articolare presenta un tronco di cono idoneo all’accoppiamento con endoprotesi, artroprotesi convenzionali, protesi inverse, o megateste rotante; 2) gli elementi articolari possono essere sia di dimensioni ristrette (per accoppiamento con trapianti osteotendinei ovvero protesi composite) sia a volume anatomico e di varie dimensioni; 3) presenza di vite verticale di connessione per controllo delle rotazioni; 4) fori perimetrali e aree a porosità superficiale per l’ancoraggio della cuffia dei rotatori.
Nell femore distale o nella tibia prossimale, o in genere nelle resezioni di ginocchio (in cui vengono totalmente sacrificati i legamenti collaterali, la capsula e i crociati) l’articolazione viene ricostruita con uno snodo completamente vincolato (a cerniera) talora con limitate capacità rotazionali (sferocentrico, rotating hinge, SLE, etc) che garantiscono una completa stabilità in varo valgo. Viene privilegiato un fulcro arretrato così da garantire una stabilità in iperestensione e controbilanciare eventuali deficit stenici della muscolatura quadricipitale. Nelle protesi di femore distale non è necessario avere fori per ancoraggi muscolo-tendinei (in quanto queste strutture passano tutte a ponte sull’articolazione).
Nelle ricostruzioni di tibia prossimale, invece, il tendine rotuleo deve essere reinserito sulla protesi con una giusta tensione, al fine di garantire una efficace trasmissione delle forze esercitate dal quadricipite e preservare la funzionalità dell’apparato estensore: vi sono quindi sia fori per l’ancoraggio temporaneo dei flessori mediali, sia fori per placche di ancoraggio a livelli diversi del tendine rotuleo
Segmenti intercalari
Le zone intercalari vengono ricostruite con uno o più segmenti cilindrici raccordati fra loro e che vanno a determinare con la componente articolare la lunghezza finale dell’impianto. Di solito tali cilindri hanno dimensioni crescenti di 2cm in 2cm. L’introduzione di una componente dispari (3cm) permette di sostituire il segmento resecato con accuratezza centimetrica. I sistemi attualmente a disposizione permettono di sostituire tutto il femore e i due terzi della tibia all’arto inferiore e tutto l’omero e il gomito all’arto superiore.
I vari segmenti si connettono fra loro con semplici connessioni coniche. Nei modelli iniziali erano molto lunghe (fino a 6 cm): attualmente sono molto più corte (2-3 cm) per permettere un disassemblaggio più facile. Tali coni non devono avere punti di minor resistenza (fori per viti stabilizzatrici): la stabilità in rotazione viene incrementata con vari artifici (linguette esterne che si incastrano nel segmento successivo; connessioni con incastri a Z della base; configurazione ovale del cono etc). Tali connessioni coniche possono dopo lungo tempo imparentarsi (fusione a freddo) ed esserci difficoltà nella loro disconnessione nelle revisioni successive: per tale motivo ogni sistema deve possedere una strumentazione adatta per il disassemblaggio delle componenti
Di norma, i segmenti intercalari sono lisci. Viene fatta eccezione, al termine del segmento diafisario, nel punto di contatto con l’osso ricevente ove può essere inserito un cilindro di transizione con superficie ruvida o trabecolata (alcune protesi portano invece tale zona inserita alla base dello stelo) Questo collare viene ivi posizionato per creare una cicatrice che isoli e sigilli il canale midollare, impedendo comunicazioni tra quest’ultimo e l’ambiente peri-protesico. Ciò minimizza il rischio che detriti (di polietilene, di metallo o di altra natura) si infiltrino nel canale diafisario all’interfacccia osso/ cemento /stelo prevenendo così mobilizzazioni asettiche e fallimenti degli impianti (effetto “stringa”).
Nell’arto superiore questi segmenti intercalari sono cavi all’interno e presentano una superfice con vari fori passanti: questo artifizio è dovuto alla necessità di diminuire al massimo il peso della protesi e per fornire una area dove passare legamenti artificiali ove reinserire i muscoli.
La connessione di vari segmenti fra loro con una componente di raccordo centrale permette di eseguire anche ricostruzioni intercalari o artrodesizzanti. Questo permette, in caso fosse richiesto, di convertire in un secondo tempo una resezione articolare di ginocchio in artrodesi (insufficienza quadricipitale) o una resezione di femore prossimale o distale in protesi totale di femore lasciando in situ la maggior parte dei componenti della protesi iniziale.
Steli Protesici
- Lo stelo protesico, serve a solidarizzare la megaprotesi all’osso nel quale viene impiantata.
- Un valido sistema dovrebbe prevedere sia steli cementati che non cementati intercambiabili fra loro. Gli steli non cementati sono indicati nei pazienti giovani, con tumori primitivi, buon stock osseo, con osso non precedentemente irradiato né prevista radioterapia futura, e in cui si è ottenuto un adeguato press fit intraoperatorio. Gli steli cementati sono preferiti nei pazienti anziani, osteoporotici, nelle metastasi, in osso precedentemente irradiato o che potrà essere irradiato e quando il press fit di uno stelo non cementato risulti insufficiente.
- Gli steli cementati spesso presentano un anello poroso tridimensionale alla loro base per ottenere l’effetto purse string. All’arto inferiore (ove insistono stress in compressione e in rotazione) la sezione trasversa di tali steli è quella convenzionale delle protesi da revisione a stelo lungo (clover leaf). All’omero possono invece avere sia scanalature verticali che trasversali per resistere meglio anche a stress in trazione tipici di tale distretto.
- Gli steli non cementati possono essere di morfologia tronco conica con sezione stellata (tipo Wagner) o cilindrica anatomica a contatto totale (curvi nel femore) o retti con tre punti di contatto.
- Fori passanti attraverso lo stelo per garantirne la stabilità primaria alla fine di ottenere un bone ingrowth dovrebbero essere evitati, o la loro presenza dovrebbe essere limitata al minimo e permessa solo all’arto superiore) poiché sono aree di minore resistenza e di maggior rischio di rottura dell’impianto.
- Per ottenere maggior resistenza alle forze di torsione alcuni steli hanno alla base una configurazione sfaccettata (esagonale o ottagonale) che prevede un accurato e laborioso alloggiamento nella zona diafisaria ricevente. Altri steli (tronco conici) confidano nel contatto per almeno 5 cm della loro configurazione a stella con la corticale, nel loro sempre maggior contatto periferico in caso di micro affondamento sotto carico e su plug periferici alla base dello stelo che si incastrano su nicchie create nella corticale ossea a livello della osteotomia. Sempre per assorbire gli stress rotazionali possono essere utilizzate flange esterne alla corticale a incastro (o eventualmente fissate con viti monocorticali non passanti): accorgimento tecnico usato con successo nelle resezioni di gomito.
- Per ridurre il rischio di fratture iatrogene a carico della diafisi e garantire il miglior fit dello stelo, lo strumentario della megaprotesi deve disporre di frese e steli che vadano di millimetro in millimetro, senza costringere il chirurgo a pericolose approssimazioni.
- Un fallimento meccanico della protesi è attualmente evento raro (1%) ma non in passato (5-7%). Una rottura dello stelo era associata a:
- steli di piccolo calibro (10 mm);
- peso del paziente oltre 80 kg;
- presenza di fori nei primi 5 cm dello stelo o fori passanti attraverso i raccordi conici
- sede: più frequenti nelle resezioni di femore distale (più la resezione è lunga più lo stelo si allontana dall’asse di carico ed è sottoposto a maggiori stress flettenti); più rari nelle resezioni di femore prossimale (più la resezione è lunga più lo stelo si avvicina all’asse di carico ed è sottoposto a minori stress flettenti); quasi inesistenti nelle resezioni di tibia (ove lo stelo coincide con l’asse di carico).
- entità del muscolo quadricipite asportato: il paziente anche dopo exeresi subtotale di tale muscolo può camminare lanciando l’arto con l’iliopsos e stabilizzando il ginocchio in iperestensione durante il carico grazie alla protesi vincolata con perno retroposto (in maniera simile alla deambulazione di pazienti amputati). Tale tipo di deambulazione determina importanti stress articolari con usura delle componenti e possibili rotture a fatica. L’usura delle componenti in polietilene (un tempo elevato) è attualmente paragonabile a quelli degli impianti standard ortopedici.
- Un fallimento settico è presente in circa il 10% dei casi: tale valore è comparabile a quello dei trapianti massivi con cui ne condivide le concause. Un vantaggio delle megaprotesi può essere quello di un rivestimento in argento (che avrebbe la possibilità di prevenire il biofilm batterico) 5,6.
PROTESI CUSTOM MADE
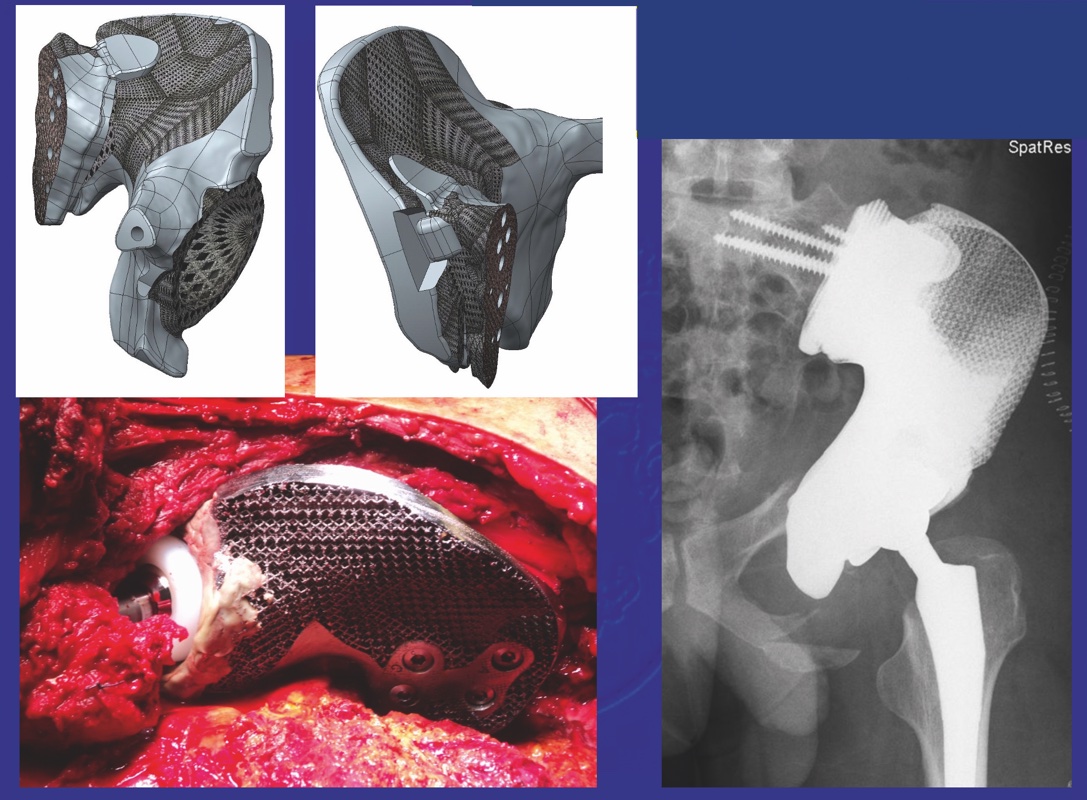
Negli ultimi anni, le innovazioni dell’additive engineering e della stampa in 3D, hanno consentito l’introduzione di moderne protesi custom made. Queste protesi riproducono fedelmente l’anatomia di un singolo paziente, basandosi su acquisizioni preoperatorie di TAC e Risonanze Magnetiche dell’osso da ricostruire o del suo controlaterale (mirroring). Sebbene impiegate per riprodurre qualsiasi segmento dell’apparato muscoloscheletrico, hanno trovato il loro più largo utilizzo nella ricostruzione del cingolo pelvico e scapolare. Nella pelvi un design customizzato garantisce evidenti vantaggi rispetto a protesi di natura modulare, che non potrebbero riprodurre fedelmente una struttura a sviluppo poliassiale (Fig. 4)
L’utilizzo delle protesi custom made presuppone le seguenti fasi:
Planning
Pianificazione pre-operatoria. Un fitto confronto tra chirurghi ed ingegneri deve portare ad identificare con precisione forma e dimensioni del difetto osseo. Devono essere scelti accuratamente anche le sedi ed i metodi di ancoraggio della protesi a ciò che resta dell’osso nativo. La forma e le dimensioni del difetto osseo vengono acquisite grazie ad immagini TC ed RM del singolo paziente. Si può prendere come riferimento anatomico l’osso stesso che si intende convertire in protesi oppure, qualora questo sia marcatamente deformato, si può sfruttare l’osso controlaterale, specchiandolo ed adattandolo al sito ricevente. Le linee di taglio vengono concordate in fase di planning. Queste devono consentire una resezione ampia dell’osso malato, e garantire un combaciamento stabile e immediato (nel punto desiderato e solo in quello) tra protesi e osso.
Design
Il design della protesi, delle linee di taglio e dei modelli di prova (phantom) rappresenta una parte fondamentale della chirurgia custom made.
- Modelli di prova in plastica non sterili devono essere forniti al chirurgo per prendere dimestichezza con la protesi definitiva preoperatoriamente ma soprattutto copie sterili devono poter essere usate in sede intra-operatoria per controllare la bontà della resezione.
- Apposite guide di taglio possono essere utilizzate per praticare l’osteotomia nel punto esatto stabilito nel planning pre-operatorio. Sebbene le guide di taglio siano fondamentali, il loro design è spesso controverso. Guide con una larga base d’impianto sull’osso consentono una maggiore precisione, ma presuppongono maggiore esposizione e traumatismo a carico del periostio e dei tessuti molli limitrofi. D’altro canto, guide di taglio strette richiedono meno esposizione ossea, ma sono instabili e conferiscono una precisione subottimale del taglio. Vi sono poi sedi in cui il posizionamento delle guide di taglio sarebbe rischioso per la presenza di strutture vascolo nervose (sacroiliaca, incisura ischiatica, triangolo inguinale) per cui è utile ricorrere alla navigazione.
- Le protesi custom made vengono disegnate con una forma che globalmente riproduce quella dell’osso nativo. La protesi deve prevedere superfici lisce che scoraggino l’aderenza coi tessuti contigui nelle aree a contatto con organi splancnici, vasi e nervi maggiori (nel bacino la branca ileopubica, l’articolazione sacroiliaca e la grande incisura ischiatica). Nello stesso tempo deve prevedere una porosità tridimensionale nelle zone a contatto con l’osso (zona osteotomica) e i muscoli per favorire la crescita ossea, per migliorare l’adesione dei tessuti molli, per alleggerire la protesi ed eventualmente per caricare le superfici con antibiotici (Jodine, argento) per prevenire infezioni.
- I siti di ancoraggio devono supportare il costrutto protesi-osso e limitare al minimo il rischio di cedimento. La protesi si deve quindi ancorare a segmenti ossei spessi e resistenti, quali la zona sovraacetabolare, il tratto sacro-iliaco e la linea innominata.
- La fissazione tra protesi ed osso deve essere accuratamente selezionata sulla base della zona da protesizzare. Protesi periacetabolari, ad esempio, possono basarsi su ancoraggi triflangiati, che distribuiscano le forze su ilio, ischio e pube. Nei casi con resezione sovraacetabolare (in cui viene conservato esclusivamente l’osso iliaco) si più ricorrere invece ad uno stelo modulare tipo McMinn (“Ice cone / pedestal cup”) con l’aggiunta di uno o più steli ausiliari con finalità antirotazionali. Nei casi in cui il corpo dell’ilio è rimosso o in buona parte sacrificato, si può invece ricorrere a sistemi di steli, placche e viti che solidarizzino la protesi alla restante ala iliaca (quando presente) ma soprattutto si spingano ad ancorarsi con placche flangiate alla zona più spessa della sacroiliaca. Le resezioni dell’emibacino con sezione verticale della sacroiliaca sono le più difficoltose e richiedono barre transsacrali o estensioni spino pelviche con esiti incerti.
Intervento chirurgico
L’intervento chirurgico può essere svolto in un singolo tempo, oppure in due tempi.
Negli interventi in un unico tempo chirurgico, alla fase di resezione segue immediatamente quella di ricostruzione. Questo approccio consente di limitare i tempi chirurgici complessivi e il ricovero ospedaliero, ma presume un tempo rapido di design e di produzione (per evitare progressione tumorale) e riduce al minimo il margine di errore o di variazione da parte del chirurgo (la protesi non è modificabile e non si può eseguire un re-cut in caso di margini positivi per malattia).
Negli interventi in due tempi, viene eseguita dapprima la parte demolitiva con apposizione temporanea di cemento spaziatore mentre nel postoperatorio viene eseguito il planning per la elaborazione della protesi che verrà montata a distanza di tempo.I vantaggi di una procedura in due tempi in oncologia sono: 1) in primo luogo non perdere tempo per aspettare la protesi; in secondo luogo, in seguito al controllo dei margini, programmare ed eseguire un eventuale ampliamento degli stessi (se risultassero non adeguati) in corso dell’intervento definitivo. Nella chirurgia di revisione. 1) la rimozione della protesi metallica comporta un minor numero di artefatti e uno studio più accurato 2) avendo rimosso la protesi, la perdita ossea è quella reale, non quella presunta 3) il letto chirurgico viene ripulito e verificata l’assenza di infezione 4) Migliore controllo delle complicanze della ferita7,8.
CAPITOLO 96Bibliografia.
- Archual AJ, Bishop AT, Shin AY. Vascularized Bone Grafts in Orthopaedic Surgery: A Review of Options and Indications. J Am Acad Orthop Surg. 2022 Jan 15;30(2): 60-69. doi: 10.5435/JAAOS-D-20-01200.
- Baldwin P, Li DJ, Auston DA, et al. Autograft, Allograft, and Bone Graft Substitutes: Clinical Evidence and Indications for Use in the Setting of Orthopaedic Trauma Surgery. J Orthop Trauma. 2019 Apr;33(4): 203-213. doi: 10.1097/BOT.0000000000001420.
- Aro HT, Aho AJ. Clinical use of bone allografts. Ann Med. 1993 Aug;25(4): 403-12. https://doi.org/10.3109/07853899309147303.
- Delloye C, Cornu O, Druez V, et al. Bone allografts: What they can offer and what they cannot. J Bone Joint Surg Br. 2007 May;89(5): 574-9. doi: 10.1302/0301-620X.89B5.19039.
- Capanna R, Scoccianti G, Frenos F, et al. What was the survival of megaprostheses in lower limb reconstructions after tumor resections? Clin Orthop Relat Res. 2015 Mar;473(3): 820-30. doi:10.1007/s11999-014-3736-1.
- Vaishya R, Thapa SS, Vaish A. Non-neoplastic indications and outcomes of the proximal and distal femur megaprosthesis: a critical review. Knee Surg Relat Res. 2020 Apr 9;32(1): 18. doi:10.1186/s43019-020-00034-7.
- Angelini A, Trovarelli G, Berizzi A, et al. Three-dimension-printed custom-made prosthetic reconstructions: from revision surgery to oncologic reconstructions. Int Orthop. 2019 Jan;43(1): 123-132. doi:10.1007/s00264-018-4232-0.
- Andreani L, Ipponi E, Neri E, et al. 3d printing in orthopedic oncology surgery. Minerva Orthop 2021;72:352-8. doi: 10.23736/S2784-8469.21.04057-8.
Materiale Supplementare
Disponibile al link: https://drive.google.com/drive/folders/1d1Nm2Z0wRE0rlb-3RTQK-6dOF8qqu1ob?usp = drive_link