Fondamenti delle lesioni legamentose del ginocchio
1 UOC Ortopedia, Policlinico Umberto I, Università di Roma “La Sapienza”, Roma; 2 Istituto Dermopatico dell’Immacolata, Roma
ANATOMIA
Il legamento crociato anteriore (LCA) origina sulla superficie mediale del condilo femorale esterno, decorre poi anteriormente, distalmente e medialmente verso la sua inserzione tibiale a livello della fossa intercondiloidea. La sua lunghezza media è di 32 mm, con un diametro medio di 11 mm.
È costituito da due fasci:
-
antero-mediale: è il principale stabilizzatore della traslazione anteriore della tibia sul femore, risulta esser teso in flessione;
-
postero-laterale: responsabile secondariamente del controllo della stabilità rotatoria del ginocchio, risulta teso in estensione.
La vascolarizzazione è garantita dall’arteria genicolata media.
Il legamento crociato posteriore (LCP) origina dal condilo femorale mediale e si inserisce vicino al solco tibiale posteriore. Le sue dimensioni sono di 38 mm in lunghezza per 13 mm di diametro.
È costituito da due fasci:
-
antero-laterale, teso durante la flessione, rappresenta la componente più importante per la stabilità posteriore a 90° di flessione;
-
postero-mediale: teso durante l’estensione. Si trova tra i legamenti meniscofemorali, noti come legamento di Humphrey (anteriore) e legamento di Wrisberg (posteriore).
Il LCP è vascolarizzato dai rami dell’arteria genicolata mediale.
Il legamento collaterale mediale (LCM) si divide in fascio superficiale (sLCM) e profondo (dLCM). La sua origine femorale è sull’epicondilo mediale, 1 cm dal tubercolo degli adduttori. L’inserzione tibiale avviene a 4.5 cm dalla linea articolare, posteriormente al gracile. Il legamento collaterale mediale profondo è costituito dai fasci meniscofemorale e meniscotibiale.
Il legamento collaterale laterale (LCL) ha origine sull’epicondilo laterale, e si inserisce all’apice anterolaterale della testa della fibula.
BIOMECCANICA
Il legamento crociato anteriore (LCA) contrasta la traslazione tibiale anteriore e la rotazione interna. La sua maggiore tensione è tra 0° e 30° di flessione, mentre è minore tra i 60° e i 90°. Sebbene una lesione isolata del LCA sembri influire minimamente sulla rotazione interna, la rottura del LCA modifica il centro di rotazione del ginocchio, spostandolo verso il passaggio corpo-corno anteriore del menisco interno. Ciò comporta un aumento del movimento nel comparto esterno e un incremento delle forze in situ del 415% a 15° di flessione, contribuendo parzialmente all’aumentato rischio di lesioni del menisco interno nei pazienti che non si sottopongono a intervento di ricostruzione del LCA.
Il controllo della rotazione antero-laterale del ginocchio è affidata anche ad altre strutture anatomiche 1, definite come “secondary restraint” dagli anglo-sassoni, e raggruppate nel “complesso antero-laterale (fibre posteriori della banda ileo-tibiale, uno strato più profondo capsulo-osseo, le fibre di Kaplan, la capsula antero-laterale, il corno posteriore del menisco esterno e il legamento antero-laterale ALL). La descrizione del Complesso Antero Laterale del ginocchio è attribuita a Hughston 2 e Muller 3, ma il termine “legamento antero-laterale” è stato coniato da Viera nel 2007, mentre la sua descrizione anatomica è dovuta a Steven Claes 4 nel 2013. Origina dal condilo femorale esterno e si inserisce sulla tibia tra il tubercolo del Gerdy e la testa del perone.
Il LCP è il principale stabilizzatore del ginocchio nei movimenti di traslazione postero-anteriore (95%).
Il sLCM garantisce la stabilità contro lo stress in valgo a tutte le angolazioni del ginocchio, maggiormente a 25° di flessione. Tuttavia agisce anche come stabilizzatore secondario della rotazione esterna della tibia e la traslazione anteriore/posteriore della stessa. Il dLCM stabilizza maggiormente in completa estensione del ginocchio.
Il LCL è il principale stabilizzatore dello stress in varismo, intervenendo in modo significativo a 5° e 30° di flessione del ginocchio.
Si rivela altresì come uno stabilizzatore secondario alla rotazione posterolaterale quando il ginocchio è flesso meno di 50°.
MECCANISMI TRAUMATICI E LESIONI ASSOCIATE
Tradizionalmente i meccanismi traumatici che portano la lesione del LCA sono da dividere in:
-
Valgo rotazione esterna: la prima struttura ad esser messa in tensione è il legamento collaterale mediale (LCM), più precisamente il fascio superficiale, poi il LCA ed in casi più rari si ha il coinvolgimento del legamento collaterale esterno (LCL) o del legamento crociato posteriore (LCP).
-
Varo rotazione interna: la prima struttura messa in tensione è il LCA, seguito dalle strutture antero-laterali e dal LCL, spesso viene coinvolto il corno posteriore del menisco esterno, più raramente il mediale.
-
Iperflessione: tendenzialmente comporta la lesione del corno posteriore del menisco interno, ma qualora si assista alla brusca contrazione del quadricipite si può avere una traslazione anteriore della tibia su femore che causa la rottura del LCA.
-
Iperestensione: più frequentemente coinvolge il LCP, ma in alcuni casi si può avere una lesione isolata del LCA con un meccanismo a “Ghigliottina” nella gola femorale.
Ma la frequente associazione di lesioni delle strutture antero-laterali (circa il 90% come dimostrato in vivo da Ferretti et al. 5) alla lesione acuta del LCA, ha spinto molti autori a prendere in considerazione un nuovo meccanismo traumatico definito “pivot shift like” in cui la lesione del LCA avviene nei primi 40 ms con meccanismo traumatico in valgo, accompagnato da una intra-rotazione tibiale (in grado di provocare la sublussazione anteriore del piatto tibiale esterno e la conseguente rottura del LCA) e seguito da una extra-rotazione 6.
Il termine “unhappy triad” è stato coniato per la prima volta nel 1964 da O’Donoghue 7, identificando, in circa il 25% degli infortuni acuti al ginocchio negli atleti, la lesione del LCA, del LCM e del il menisco mediale.
DIAGNOSI CLINICA E STRUMENTALE
La diagnosi delle lesioni legamentose è prevalentemente clinica. In primo luogo il paziente associa al trauma distorsivo una sensazione di “crack” e di instabilità del ginocchio. Altro dato da non sottovalutare è l’emartro, che si sviluppa solitamente 12 ore dopo la lesione.
Test clinici per una corretta e completa valutazione articolare sono:
-
Lachman test: con il ginocchio flesso a 30° il femore viene tenuto con una mano dall’operatore, mentre l’altra traziona la tibia in avanti. È il test più specifico per il LCA.
-
Pivot shift: viene eseguito con il paziente supino, si esegue l’intrarotazione della gamba e l’applicazione di un valgo stress, rivelandosi positivo quando si percepisce uno scatto durante il passaggio dalla flessione all’estensione.
-
Valgo stress a 30°: serve per valutare l’integrità del LCM, si esegue sempre in comparativa con il lato sano. Il paziente è in posizione supina con il ginocchio flesso a 30° fuori dal lettino. Si applica un valgo stress al ginocchio per valutare il grado di lassità.
-
Varo stress a 30°: serve per valutare l’integrità del LCL, si esegue sempre in comparativa con il lato sano. Il paziente è in posizione supina con il ginocchio flesso a 30° fuori dal lettino. Si applica un varo stress al ginocchio per valutare il grado di lassità.
Gli artrometri, come il KT-1000 ed il KT-2000, permettono di quantificare la traslazione tibiale anteriore applicando diversi gradi di forza fino alla “maximum manual load” e di valutare “side to side” (S/S) le differenze. Una differenza S/S > 3 mm è indicativa di lesione del LCA.
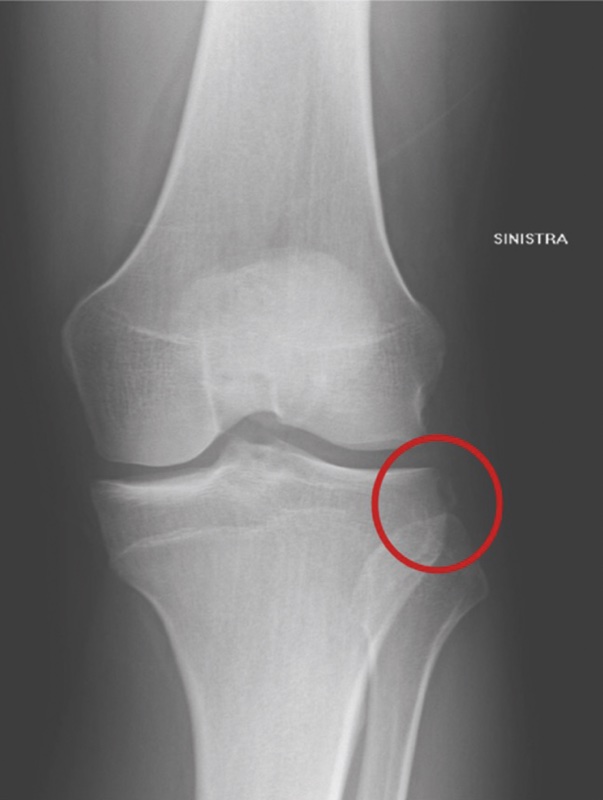
La valutazione radiografica sicuramente può fornire ulteriori informazioni, oltre che identificare altre lesioni. Nelle radiografie con proiezione AP si può evidenziare la frattura di Segond (Fig. 1) 8, segno indiretto di lesione del LCA in cui si ha l’avusione nel piatto tibiale esterno di un piccolo frammento da parte del legamento antero-laterale.
TRATTAMENTO CHIRURGICO
La decisione di sottoporsi all’intervento chirurgico dovrebbe tener conto di variabili cruciali come l’età del paziente, l’attività sportiva, il grado di instabilità rotatoria e la presenza di lesioni associate, in particolare quelle meniscali.
TECNICHE CHIRURGICHE DI RICOSTRUZIONE
Le tecniche di ricostruzione del Legamento Crociato Anteriore (LCA) comportano una scelta cruciale 9: l’utilizzo di autotrapianti o allografts. Mentre gli allografts sono associati a una maggiore incidenza di fallimenti, specialmente nei giovani sportivi, gli autotrapianti (tendine rotuleo – BPTB, semitendinoso e gracile – HS, tendine quadricipitale – QT) mostrano risultati comparabili, e la scelta spesso dipende dall’esperienza del chirurgo.
Il BPTB è stato a lungo considerato il “gold standard”, ma l’uso degli hamstring è cresciuto notevolmente negli ultimi 10 anni, e attualmente risulta il più utilizzato. La ricostruzione con tendine rotuleo presenta svantaggi come il dolore anteriore del ginocchio, un’incidenza maggiore di artrosi femoro-rotulea e rischi di fratture rotulee e lesioni del tendine.
L’utilizzo degli hamstring comporta meno dolore post-operatorio, ma può presentare complicazioni legate alla fissazione al di fuori dei tunnel, causando il rischio di allungamento del trapianto (effetto bungee) e mancanza di contatto osso-osso, che prolunga il tempo di guarigione biologica rispetto all’autotrapianto con tendine rotuleo.
Nonostante ciò, gli hamstring mostrano una minore forza di flessione a breve termine, che diviene non significativa a 12 mesi grazie ai meccanismi di riparazione del sito del prelievo. Un altro svantaggio è la possibilità di un’area di ipoestesia nella sede del prelievo, evitabile con un’incisione chirurgica più obliqua.
La scelta tra autotrapianto e allograft richiede una valutazione ponderata delle variabili, tra cui età del paziente, attività sportiva e lesioni associate, per determinare la soluzione più adatta alle esigenze individuali.
Per quanto riguarda i mezzi di fissazione il mercato sicuramente fornisce un’ampia scelta. I devices sono da dividere in:
-
a compressione (vite ad interferenza);
-
a espansione (rigidfix);
-
a sospensione:
-
corticale: sintetici a loop (Tight rope, Endobutton), metallici (swing bridge);
-
spongiosa: (Lynx HT);
-
cortico-spongiosa (Transifix).
Il tunnel tibiale si esegue con utilizzo di apposita guida “a compasso” con un angolo di apertura attorno ai 50-60°.
Il tunnel femorale può esser eseguito con diverse tecniche:
-
antero-mediale: Si utilizzano quindi delle apposite guide con off-set a seconda del diametro del trapianto;
-
out-in: Uno dei principali vantaggi è che il posizionamento del tunnel è indipendente da quello tibiale e può esser meglio posizionato. Si incide longitudinalmente la fascia lata 2 cm anteriormente al suo margine posteriore, si separa il vasto laterale dal setto intermuscolare e lo si divarica verso l’alto con un divaricatore dedicato. Dal portale si applica la guida femorale, nella posizione voluta (ore 10 per il ginocchio destro, ore 2 per il sinistro);
-
in-out (trans-tibiale): il tunnel femorale viene eseguito direttamente attraverso il tunnel tibiale.
TECNICHE CHIRURGICHE DI RIPARAZIONE
Sebbene in passato siano stati riportati alcuni casi sporadici di guarigione spontanea, le lesioni del LCA sono oggi abitualmente trattate con trapianti tendinei autologhi (Tendine rotuleo, tendini flessori, tendine quadricipitale).
In realtà la riparazione diretta delle lesioni dell’LCA fu la prima tecnica chirurgica utilizzata, risalendo addirittura al 1903 3. Tuttavia gli scarsi risultati clinici avevano portato alla convinzione che il LCA, una volta rotto, fosse di fatto irreparabile e richiedesse in ogni caso la sua sostituzione con un trapianto.
In alcuni casi selezionati oggi è possibile, ricorrendo a nuove tecniche e materiali ad elevata resistenza, riparare il residuo del LCA mediante reinserzione artroscopica.
La variabile fondamentale da considerare nella selezione dei casi idonei alla riparazione è la sede della lesione.
Sede della lesione
Le lesioni dell’LCA sono state classificate da Shermann et al. 10 in base alla sede in quattro tipi. Il tipo I include le lesioni al tetto, in prossimità dell’origine del LCA sul condilo femorale esterno. Il tipo II quelle al terzo prossimale. Il tipo III quelle a metà (50% di lunghezza del moncone distale) e quelle IV distali con un moncone più corto del 50%. È stato documentato come la sede della rottura sia statisticamente correlata all’età, essendo le rotture prossimali più frequenti negli adulti 11.
Il principale compito della chirurgia sarebbe quindi quello di riaccostare i monconi, ripristinando la normale anatomia e tensione del legamento. Sebbene le moderne biotecnologie appaiano in grado di stimolare le diverse fasi del processo riparativo (scaffold biomimetici, fattori di crescita etc.) 12 appare ragionevole pensare che un intervento molto precoce, quando l’organismo è in grado di esprimere la sua massima potenzialità riparativa, offra le maggiori probabilità di successo.
Le revisioni della letteratura e meta-analisi riportano tassi di successo che oscillano dal 53% al 100% con risultati estremamente positivi quando si considerano le tecniche più recenti, seppur con follow-up a breve termine 13-14.
TRATTAMENTO DELLE LESIONI ASSOCIATE
-
LCM: Il trattamento della lesione del LCM si adatta alla gravità della lassità. La ricostruzione del LCA è prioritaria nelle lassità moderate (+ o ++), mentre nelle lassità marcate (+++) coinvolge sia il pivot centrale che il LCM. La procedura chirurgica è principalmente artroscopica, ma in caso di complessità, l’esplorazione open è considerata, con la possibile complicanza di calcificazioni (malattia di Pellegrini-Stieda). Nel trattamento post-operatorio va valutata l’astensione dal carico per 3/4 settimane.
-
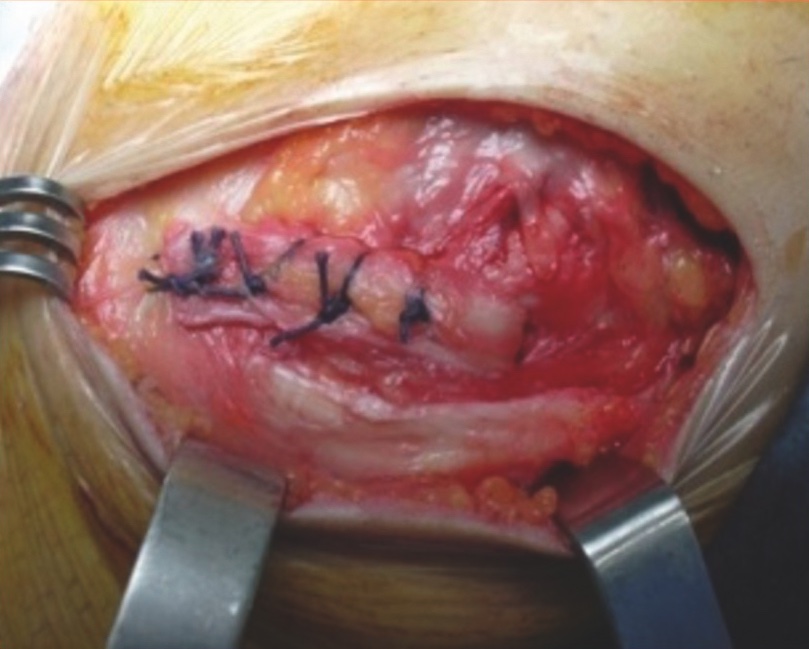
Complesso antero-laterale: il trattamento delle lesioni del Complesso Antero-Laterale, spesso associato alle lesioni del LCA, in acuto si esegue riparando direttamente il danno con punti staccati. Le ricostruzioni del ALL possono esser anatomiche (con fascia lata, gracile…) o non anatomiche (tenodesi o plastiche periferiche): molto utilizzata è la McIntosh Cocker-Arnold modificata (Fig. 2), in cui una porzione di fascia lata lunga circa 10 cm e larga 1 cm viene fatta passare sotto il LCL e ribaltata verso il tubercolo del Gerdy e suturata con il piede in rotazione esterna. Le indicazioni alla plastica periferica sono: pazienti di sesso femminile, interventi di revisione, atleti ad alto rischio, instabilità rotatoria 3+, iperlassità legamentosa.
COMPLICANZE
Attualmente l’incidenza di insuccesso può variare dal 3 al 24%.
Le cause di una recidiva di lassità dopo ricostruzione primaria sono classificabili in 2 gruppi: traumatiche e atraumatiche.
-
Cause traumatiche. Un nuovo trauma simile in entità a quello del primo infortunio può determinare la rottura del trapianto.
-
Cause atraumatiche. Le cause atraumatiche sono rappresentate da errori tecnici, fattori biologici e errori diagnostici.
-
Gli errori tecnici sono la causa più comune di fallimento sono principalmente dovuti al malposizionamento dei tunnel.
-
Fattori biologici. Il processo di maturazione biologica del trapianto (necrosi, rivascolarizzazione e maturazione) è facilmente alterato da fattori meccanici (sovratensionamento del trapianto, immobilizzazione post-operatoria), o biologici (infezione, o reazione immunologica avversa nel caso di allotrapianti).
-
Errori diagnostici. La rottura del legamento crociato anteriore è spesso associata a lesioni capsulari e legamentose periferiche. Instabilità non diagnosticate o non trattate al tempo della prima ricostruzione, possono portare ad un progressivo deterioramento del neo LCA con recidiva della lassità anteriore.
Le complicanze dell’intervento di ricostruzione del LCA si dividono in:
-
Intra-operatorie:
-
frattura della rotula (propria del BPTB);
-
caduta del graft: utile disinfezione in una soluzione di clorexidina gluconata e soluzione antibiotica (gentamicina, polimixina e clindamicina);
-
mal posizionamento dei tunnel sul piano sagittale (70% dei fallimenti);
-
mal posizionamento dei tunnel sul piano sagittale: Graft troppo verticale determina una instabilità rotatoria;
-
lesione del trapianto durante il prelievo (HS);
-
trapianti troppo corti o sottili;
-
mancato tensionamento del graft: instabilità rotatoria;
-
insufficiente fissazione del trapianto;
-
post-operatorie:
-
artrofibrosi e perdita del ROM: principale complicanza, maggiore nei casi. Nelle prime 12 settimane normalmente si esegue una intensa chinesi mirata al recupero del ROM, oltre questo momento si procede alla sblocco in narcosi o eventuale lisi artroscopica delle aderenze;
-
infezioni: spesso legate a S. Epidermidis si manifestano con dolore, tumefazione, aumento dei globuli bianchi nei primi 14 giorni dall’intervento. Il trattamento normalmente si risolve con un lavaggio artroscopico ed una antibiotico terapia mirata per 6 settimane;
-
emartro;
-
rottura del tendine rotuleo (propria del BPTB);
-
algodistrofia locale;
-
frattura della rotula: generalmente occorre 8-12 settimane dopo il BPTB;
-
osteolisi;
-
artrosi tardiva;
-
anestesia locale per lesione del nervo safeno durante il prelievo degli HS;
-
sindrome del ciclope: proliferazione di tessuto fibrovascolare che causa dolore nell’estensione;
-
trombosi venosa profonda che può provocare l’embolia polmonare.
CAPITOLO 70Bibliografia.
-
Amis AA. Anterolateral knee biomechanics. Knee Surg Sports Traumatol Arthrosc. 2017;25(4):1015-23. doi: 10.1007/s00167-017-4494-x.
-
Hughston JC, Andrews JR, Cross MJ, et al. Classification of knee ligament instabilities. Part I. The medial compartment and cruciate ligaments. J Bone Joint Surg Am. 1976;58(2):159-72.
-
Muller W. The knee. New York: Springer-Verlag; 1983.
-
Claes S, Vereecke E, Maes M, et al. Anatomy of the anterolateral ligament of the knee. J Anat. 2013;223:321-8. doi: 10.1111/joa.12087.
-
Ferretti A, Monaco E, Fabbri M, et al. Prevalence and classification of injuries of anterolateral complex in acute anterior cruciate ligament tears. Arthroscopy. 2017;33(1):147-54. doi: 10.1016/j.arthro.2016.05.010.
-
Koga H, Bahr R, Myklebust G, et al. Estimating anterior tibial translation from model-based image-matching of a noncontact anterior cruciate ligament injury in professional football: a case report. Clin J Sport Med. 2011;21(3):271-4. doi: 10.1097/JSM.0b013e31821899ec.
-
Ferretti A, Monaco E, Ponzo A, et al. The unhappy triad of the knee re-revisited. Int Orthop. 2019;43(1):223-8. doi: 10.1007/s00264-018-4181-7.
-
Segond P. Recherches cliniques et experimentales sur les epanchements sanguins du genou par entorse. Progres Med. 1879 Paris.
-
Pioger C, Gousopoulos L, Hopper GP, et al. Clinical outcomes after combined ACL and anterolateral ligament reconstruction versus isolated ACL reconstruction with bone-patellar tendon-bone grafts: a matched-pair analysis of 2018 patients from the SANTI study group. Am J Sports Med. 2022;50(13):3493-501. doi: 10.1177/03635465221128261.
-
Sherman MF, Lieber L, Bonamo JR, et al. The long-term follow-up of primary anterior cruciate ligament repair: defining a rationale for augmentation. Am J Sports Med. 1991;19(3):243-55. doi: 10.1177/036354659101900307.
-
Van der List JP, Mintz DN, DiFelice GS. The location of anterior cruciate ligament tears: a prevalence study using magnetic resonance imaging. Orthop J Sports Med. 2017;5(6):2325967117709966. doi: 10.1177/2325967117709966.
-
Gobbi A, Whyte GP, Saithna A, et al. Primary anterior cruciate ligament repair with hyaluronic scaffold and autogenous bone marrow aspirate augmentation in adolescents with open physes. Arthrosc Tech. 2019;8(12):e1561-8. doi: 10.1016/j.eats.2019.08.016.
-
Kandhari V, Smith JJ, Patel N, et al. Clinical outcomes of arthroscopic primary anterior cruciate ligament repair: a systematic review from the Scientific Anterior Cruciate Ligament Network International study group. Arthroscopy. 2020;36(2):594-612. doi: 10.1016/j.arthro.2019.09.021.
-
Nwachukwu BU, De Bellis N, Erickson BJ, et al. Anterior cruciate ligament repair outcomes: an updated systematic review of recent literature. Arthroscopy. 2019;35(7):2233-47. doi: 10.1016/j.arthro.2019.04.005.